实验室有两瓶无标签的无色透明溶液,分别是硫酸钠和氯化钾。请回答下列问题:
(1)检验这两种溶液,通常选用氯化钡溶液而不用硝酸银溶液,理由是 ;
(2)取样,滴入氯化钡溶液,若有白色沉淀生成,则检验的样品应该是 ,反应后所得到的溶液中一定含有的溶质是 ;为检验上述溶液反应后,还可能含有的其他溶质,过滤取滤液,进行以下实验,完成下表:
| 实验操作 | 现象 | 结论 |
| 取少量滤液,滴加氯化钡溶液 | 无白色沉淀 | 反应后溶液中溶质还含有 |
| 另取少量滤液,滴加 溶液 | 有白色沉淀[来源:学科 |
(3)为鉴别硫酸钠和氯化钾溶液,除用滴加试剂的方法外,还可以采用的方法是 。
化学实验常有不同的现象,请完成下表:
| 实验操作 | 实验现象 | 反应化学方程式 |
| 铁丝在氧气中燃烧 | | |
| 碳酸钠溶液和氢氧化钙溶液混合 | | |
| 氢氧化铜粉末中滴加盐酸 | | |
有一瓶久置的氢氧化钠溶液。
(1)氢氧化钠溶液露置于空气中容易变质,请写出相关反应的化学方程式: 。变质后的产物俗称为 。
(2)取少量该溶液于试管中,向溶液中滴加无色酚酞试液,试液变红色,由此 (填 “能”或“不能”)得出氢氧化钠溶液变质。请说明判断的理由 。
(3)为探究氢氧化钠溶液是全部变质还是部分变质,设计如下表实验:
[提供信息]:a.在水中的溶解性:Ba(OH)2可溶、Ca(OH)2微溶、BaCO3难溶;
b.BaCl2溶液、Ba(NO3)2溶液、CaCl2溶液、Ca(NO3)2溶液、NaNO3溶液均显中性。
| 实验步骤 | 实验现象 | 实验结论 |
| Ⅰ.取少量该溶液于试管中,向溶液中滴加过量的 溶液,并不断振荡。 | 有 生成。 | 说明原溶液中一定有碳酸钠。 |
| Ⅱ.取步骤Ⅰ试管中的少量上层清液,滴加酚酞溶液。 | 溶液变红色。 | 说明原溶液中一定有 。 |
由以上实验可知,氢氧化钠溶液 (填“部分”或“全部”)变质。
可用于治疗胃酸过多的物质是
| A.NaCl | B.CaO | C.Al(OH)3 | D.NaOH |
对比学习有利于发现事物的共性与个性。为探究酸的化学性质,同学们进行了如下实验。
| 实验内容 |  |  |  |
| 实验现象 | A试管内无明显现象,B试管中镁带表面观察到的现象是 。 | C、D两试管中均观察到有气泡产生。 | E试管中观察到的现象是 ; F试管中无明显现象。 |
| 结论 | 酸的很多反应通常在水溶液中才能完成。 | 不同的酸具有相似的化学性质。 | 不同的酸根会导致酸的“个性”有差异。 |
请分析上述现象并回答:
(1)不同的酸具有相似的化学性质,这是因为酸的组成中都含有 (填元素符号)。
(2)不同的酸根会导致酸的“个性”有差异,因此,可用 鉴别盐酸和硫酸。
(3)清洗试管时,将C、F两试管中的无色液体同时倒入一个洁净的废液缸,废液缸中立刻冒气泡并出现白色沉淀。废液缸里最终产生的白色沉淀中一定含有硫酸钡,该反应的化学方程式为 ,白色沉淀中可能还含有 (填化学式)。
归纳总结是学习化学的重要方法,小明同学用图1总结了NaOH的四条化学性质(即NaOH与四类物质能够发生化学反应).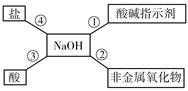
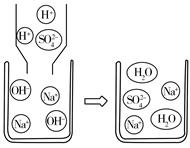
图1 图2
(1)验证反应①:小明将无色酚酞溶液滴入NaOH溶液中,溶液变成 。
(2)小明用微观示意图2来说明反应③的发生,用化学反应方程式表示为 ,从该图中可以看出,反应后的溶液pH 7(填“>”、“<”或“=”)。
(3)如果反应④能够发生,你选择的物质是 。
| A.Na2CO3 | B.HCl | C.CuSO4 | D.NaCl |

