题目内容
【题目】某校化学兴趣小组利用数字化传感器探究稀盐酸和氢氧化钠溶液的反应过程,测得烧杯中溶液的pH随滴加液体体积变化的曲线如图所示。下列说法正确的是( )
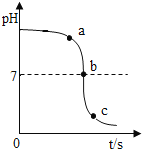
A. 图中a点所示溶液成酸性
B. 该实验是将氢氧化钠溶液逐滴滴入到盛有盐酸的烧杯中
C. b点表示盐酸与氢氧化钠恰好完全反应
D. 图中c点所示溶液中所含的溶质有NaCl和NaOH
【答案】C
【解析】
A、a点时溶液的pH大于7,溶液显碱性,故A错误;
B、pH值是开始时大于7逐渐的减小到7然后小于7,可知原溶液显碱性,然后不断的加入酸性溶液,使pH减小,说明是将稀盐酸滴加到氢氧化钠溶液中,故B错误;
C、b点等于7,所示酸和碱恰好完全发生了中和反应,故C正确;
D、c点时溶液的pH小于7,溶液显酸性,说明稀盐酸过量,所得溶液中的溶质为HCl和NaCl,故D错误。故选C。

 阅读快车系列答案
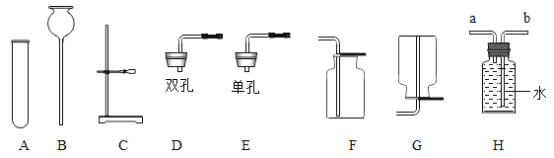
阅读快车系列答案【题目】兴趣小组为探究某些物质之间能否发生复分解反应,进行了如图所示的实验,把稀硫酸分别加入到盛有不同药品的A、B、C、D四支试管中。请回答:

(1)甲同学观察到A、B试管中均无明显现象,于是得出结论:硫酸与氢氧化钠及氯化钠都不能发生化学反应。
乙同学不同意他的观点,他认为A试管发生了复分解反应,于是补充如下方案,从“NaOH消失”的角度证明该反应的发生。

①图一方案中,加入的X可以是_____溶液(填一种即可),发生的现象为_____说明硫酸与氢氧化钠发生了化学反应。
②通过图二分析,该化学反应前后,溶液在没有发生改变的微粒是_____,该化学反应的微观实质是_____。
③甲、乙两位同学通过交流,认为稀硫酸与氯化钠溶液不能发生复分解反应的原因是_____,这也是判断溶液中能否发生复分解反应的条件。
(2)丙同学观察到C试管中有白色沉淀生成,于是得出结论:硫酸与硝酸钡发生反应,你认为该反应的微观实质是_____。
(3)丁同学观察到D试管中有气泡生成,写出该反应的化学方程式_____。
①于是该同学对反应后的D试管溶液的溶质成分进行分析得出如下结论:
结论一:K2SO4 结论二:K2SO4、K2CO3 结论三:_____
②丁同学设计实验,用两种方法验证结论三正确:
实验操作 | 实验现象 | 实验结论 | |
方法一 | 取D中溶液少许,加入足量的BaCl2溶液 | 产生白色沉淀 | 结论三正确 |
方法二 | 取D中溶液少许,加入足量的_____溶液 | _____ |
大家对方法一提出质疑,认为方法一不正确,理由是_____。
【题目】某同学按课本要求做CuSO4溶液与NaOH溶液反应的实验,有蓝色沉淀生成,对该沉淀进行加热,一般看到蓝色沉淀变黑色,可有时却看到蓝色沉淀变绿色。该同学对着异常现象产生了兴趣,决定对这现象产生的实验条件进行探究。
(查阅资料)难溶性碱受热易分解成对应的金属氧化物
写出上述生成蓝色沉淀以及蓝色沉淀变黑色的化学反应方程式:___________、__________。
(提出问题)加热蓝色沉淀没有出现黑色固体与什么因素有关?
(作出猜想)1.与CuSO4溶液过量有关;2.与NaOH溶液过量有关
(设计实验)限选试剂:1%的NaOH溶液,20%NaOH溶液,20%CuSO4溶液,1%CuSO4溶液
实验方案 | 实验现象 | 实验结论 |
1.往2mL20%CuSO4溶液中滴加2滴1%NaOH溶液,再将所得沉淀加热。 | 先产生蓝色沉淀,加热后 ______。 | 猜想1不成立 |
2._____,再将所得沉淀加热。 | 先产生蓝色沉淀,加热后 _______。 | 猜想2成立 |
(得到结论)在上述实验中,要能观察到蓝色沉淀变黑色,关键是___________
(拓展与反思)进一步查阅资料可知上述绿色物质是溶解度与氢氧化铜更小的水胆矾[化学式为Cu4(OH)6SO4],在碱性较强的条件下容易形成,继续加热一段时间该绿色固体则可产生黑色沉淀,写出该反应方程式__________.