题目内容
人类常从矿石中获取金属材料.
(1)铁是冶炼最多的金属.工业炼铁主要反应的化学方程式是: .将生锈的铁制品放入盛有稀硫酸的烧杯中,观察到溶液由无色变为黄色.写出此反应的化学方程式 .
(2)铜是人类利用较早的金属,木炭与氧化铜反应生成二氧化碳的化学方程式是 ,反应后固体的质量 (填“增大”、“减小”或“不变”)
(3)炼铝原料水铝石的主要成分是Al(OH)3,它被医疗上被用为治疗胃病的化学原理是 (用化学方程式表示).
(1)铁是冶炼最多的金属.工业炼铁主要反应的化学方程式是:
(2)铜是人类利用较早的金属,木炭与氧化铜反应生成二氧化碳的化学方程式是
(3)炼铝原料水铝石的主要成分是Al(OH)3,它被医疗上被用为治疗胃病的化学原理是
考点:铁的冶炼,酸的化学性质,碳的化学性质,书写化学方程式、文字表达式、电离方程式
专题:金属与金属材料
分析:(1)工业上通常用一氧化碳在高温的条件下来还原氧化铁制取铁;铁锈的主要成分为氧化铁,与硫酸反应属于复分解反应,生成硫酸铁和水.
(2)根据木炭的还原性来分析书写并比较固体质量的变化情况;
(3)Al(OH)3来治疗胃酸中的盐酸反应是酸碱中和反应,书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.
(2)根据木炭的还原性来分析书写并比较固体质量的变化情况;
(3)Al(OH)3来治疗胃酸中的盐酸反应是酸碱中和反应,书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.
解答:解:(1)在工业上常用一氧化碳在高温的条件下来还原氧化铁,生成铁和二氧化碳;铁锈的主要成分是氧化铁,与稀硫酸反应生成硫酸铁和水,硫酸铁溶液是黄色的.故填:Fe2O3+3CO
2Fe+3CO2;Fe2O3+3H2SO4═Fe2(SO4)3+3H2O.
(2)木炭在高温条件下和氧化铜反应原理生成铜和二氧化碳,方程式是木炭在高温条件下和氧化铜反应原理生成铜和二氧化碳,方程式是2CuO+C
2Cu+CO2↑,反应生成二氧化碳,所以固体的质量减小;故填:2CuO+C
2Cu+CO2↑;减小.
(3)Al(OH)3和胃酸中的盐酸反应是酸碱中和反应,氢氧化铝与稀盐酸反应生成氯化铝和水.该反应的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O,故答案为:Al(OH)3+3HCl=AlCl3+3H2O.
| ||
(2)木炭在高温条件下和氧化铜反应原理生成铜和二氧化碳,方程式是木炭在高温条件下和氧化铜反应原理生成铜和二氧化碳,方程式是2CuO+C
| ||
| ||
(3)Al(OH)3和胃酸中的盐酸反应是酸碱中和反应,氢氧化铝与稀盐酸反应生成氯化铝和水.该反应的化学方程式为:Al(OH)3+3HCl=AlCl3+3H2O,故答案为:Al(OH)3+3HCl=AlCl3+3H2O.
点评:书写化学方程式时,必须熟悉反应物、生成物和反应条件,必须依据客观事实、遵守质量守恒定律.

练习册系列答案
相关题目
 按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )
按如图所示装置进行实验(图中铁架台均已略去).先在试管Ⅱ中加入试剂乙,然后在试管Ⅰ中加入试剂甲,立即塞紧橡皮塞,一段时间后,观察到试管Ⅱ中有白色沉淀生成.符合以上实验现象的一组试剂是( )| A、甲:Na2CO3、稀HCl; 乙:NaOH溶液 |
| B、甲:Mg、稀H2SO4; 乙:BaCl2溶液 |
| C、甲:MgO、稀盐酸; 乙:AgNO3溶液 |
| D、甲:Cu、稀H2SO4; 乙:BaCl2溶液 |
下列过程中发生化学变化的是( )
A、 石油炼制各种产品 |
B、 浓盐酸罐车翻倒产生白雾 |
C、 自然界中的碳、氧循环 |
D、 探究燃烧的条件 |
下列四个图象中,能正确表示对应变化关系的是( )
A、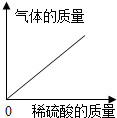 向一定量铁粉中加入稀硫酸 |
B、 一定温度下,向不饱和硝酸钾溶液中加入硝酸钾 |
C、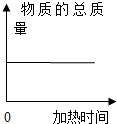 碳在密闭容器中(含空气)加热反应 |
D、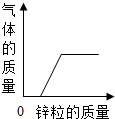 向一定量的稀硫酸和硫酸锌的混合溶液中加入锌粒 |

 化学就在我们身边,它与我们的生活息息相关.
化学就在我们身边,它与我们的生活息息相关.