题目内容
10.请根据如图所示的实验过程和提供的数据回答下列问题:
(1)第①步实验操作后,烧杯溶液中含有的溶质是(写化学式)CaCl2;
(2)在第②步实验操作中,观察到的一项实验现象是:碳酸钙固体物质不断溶解,有气体产生;
(3)计算原混合物样品中CaCl2的质量(写出计算过程,结果精确至0.1g).
分析 (1)碳酸钙不溶于水,氯化钙易溶于水,据此确定加水溶解后烧杯中溶液里含有的溶质.
(2)碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳,据此进行分析解答.
(3)加入稀盐酸时,碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳;根据质量守恒定律,烧杯内质量的减少的质量即生成的二氧化碳气体的质量,据此根据反应的化学方程式列式计算出参加反应碳酸钙的质量,进而计算出原混合物样品中CaCl2的质量.
解答 解:(1)碳酸钙不溶于水,氯化钙易溶于水,第①步实验操作后,烧杯中溶液里含有的溶质是CaCl2.故答案为:CaCl2.
(2)碳酸钙不溶于水,碳酸钙与稀盐酸反应生成氯化钙、水、二氧化碳,故在第②步实验操作中,可观察到碳酸钙固体物质不断溶解,有气体产生.故答案为:碳酸钙固体物质不断溶解,有气体产生.
(3)反应中生成CO2的质量为:13.2g+100g+100g-208.8g=4.4g.
设原混合物中CaCO3的质量为x,
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{x}=\frac{44}{4.4g}$ x=10g
原混合物样品中CaCl2的质量为:13.2g-10g=3.2g
答:原混合物样品中CaCl2的质量为3.2g.
点评 本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出二氧化碳的质量是正确解答本题的关键.

练习册系列答案
 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案 一线名师权威作业本系列答案
一线名师权威作业本系列答案
相关题目
1.填写化学方程式并简答有关的内容:
| 化学反应 | 化学方程式 | 简答 |
| 铁丝在纯氧中燃烧 | 生成物的颜色为黑色 | |
| 红磷燃烧 | 反应物的物质的量之比为4:5. | |
| 硫酸铜溶液中加入氢氧化钠溶液 | 现象:产生蓝色沉淀 | |
| 硫在氧气中燃烧 | 生成物会引起的一种环境问题是形成酸雨 |
15.下列物质中,不可能由同一种元素组成的是( )
①单质 ②氧化物③化合物 ④混合物.
①单质 ②氧化物③化合物 ④混合物.
| A. | ①② | B. | ②③ | C. | ②④ | D. | ③④ |
19.请参与某学习小组进行研究性学习的过程,并协助完成相关任务:
【提出问题】在平时探讨酸的性质时,我们通常是讨论酸的水溶液.究竟水在酸显示酸的特性时扮演什么角色呢?
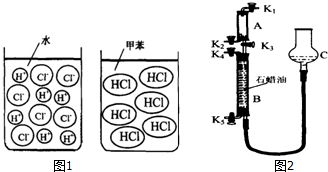
【确定研究对象】以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究.
【查阅资料】氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如图1).
【设计与实验】(请完成下表)
【讨论与反思】盐酸的酸性是因为氯化氢在水分子的作用下解离出了氢离子(H+).
水对酸显现其酸性性质非常重要.还有哪些实例或实验也可以体现水对酸显现其酸性性质的重要性呢,是否没有水,酸就不能显现酸性性质呢?(此问不作答,请在今后的学习中继续关注.)
【拓展探究】该学习小组又尝试用图2所示装置进行氯化氢气体与氨气反应的实验探究,活塞K1、K2、K3、K4、K5均关闭(装置气密性好).通过调节活塞,用排石蜡油的方法在B管中收集满了氨气.通过调节活塞K1、K2、K3,在干燥的A管中充入与大气压强相等的干燥氯化氢气体,其操作是打开K1、K2,与K2处导管口连接并通入干燥的HCl气体,集满后,先关闭K2,再关闭K1.在不用任何试剂的情况下,当看到K1导管口处有大量白雾出现现象时,说明A管中已收集满了氯化氢气体.打开K3,氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:NH3+HCl=NH4Cl•
【提出问题】在平时探讨酸的性质时,我们通常是讨论酸的水溶液.究竟水在酸显示酸的特性时扮演什么角色呢?

【确定研究对象】以我们最熟知的盐酸(氯化氢的水溶液)和氯化氢进行探究.
【查阅资料】氯化氢溶于水时解离出氢离子和氯离子,而溶于干燥的甲苯(一种有机溶剂)时仍以氯化氢分子的形式分散(如图1).
【设计与实验】(请完成下表)
| 实验内容 | 实验现象 | 解释与结论 |
| 测定导电性 | 氯化氢的水溶液:导电性良好 | 氯化氢的水溶液中有自由移动的离子 |
| 氯化氢的甲苯溶液:不导电 | 氯化氢的甲苯溶液没有自由移动的离子 | |
| 与镁作用 | 氯化氢的水溶液:有气泡产生 | 化学方程式: Mg+2HCl═MgCl2+H2↑ |
| 氯化氢的甲苯溶液:没有明显现象 | 氯化氢的甲苯溶液没有解离出氢离子 | |
| 与固态碳酸钠作用 | 氯化氢的水溶液:产生气泡 | 化学方程式:Na2CO3+2HCl=2NaCl+H2O+CO2↑ |
| 氯化氢的甲苯溶液:没有气泡产生 | 氯化氢的甲苯溶液没有解离出氢离子 |
水对酸显现其酸性性质非常重要.还有哪些实例或实验也可以体现水对酸显现其酸性性质的重要性呢,是否没有水,酸就不能显现酸性性质呢?(此问不作答,请在今后的学习中继续关注.)
【拓展探究】该学习小组又尝试用图2所示装置进行氯化氢气体与氨气反应的实验探究,活塞K1、K2、K3、K4、K5均关闭(装置气密性好).通过调节活塞,用排石蜡油的方法在B管中收集满了氨气.通过调节活塞K1、K2、K3,在干燥的A管中充入与大气压强相等的干燥氯化氢气体,其操作是打开K1、K2,与K2处导管口连接并通入干燥的HCl气体,集满后,先关闭K2,再关闭K1.在不用任何试剂的情况下,当看到K1导管口处有大量白雾出现现象时,说明A管中已收集满了氯化氢气体.打开K3,氯化氢气体与氨气发生化合反应,生成一种铵盐,写出反应的化学方程式:NH3+HCl=NH4Cl•
 水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识.请你回答:
水是人及一切生物生存所必需的,为了人类和社会经济的可持续发展,我们应该了解一些有关水的知识.请你回答: 鉴定是常用的物质检验方法之一,是根据一种物质的特殊性质,用化学方法检验它是不是这种物质.
鉴定是常用的物质检验方法之一,是根据一种物质的特殊性质,用化学方法检验它是不是这种物质.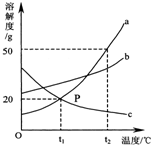 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: