题目内容
20.硝酸铵(NH4NO3)是一种常见的氮肥.请通过计算回答(1)硝酸铵的相对分子质量为80.
(2)硝酸铵中氢元素、氧元素的质量比为1:12.
分析 (1)根据相对分子质量为构成分子的各原子的相对原子质量之和,进行分析解答.
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:(1)硝酸铵的相对分子质量为14×2+1×4+16×3=80;
(2)硝酸铵中氢元素、氧元素的质量比为(1×4):(16×3)=1:12;
故答案为:(1)80;(2)7:2
点评 本题难度不大,考查同学们灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案 孟建平名校考卷系列答案
孟建平名校考卷系列答案
相关题目
12.下列各组离子在pH=2溶液中一定能大量共存的是( )
| A. | Na+ Cl- OH- | B. | Ag+ Cl- NO3- | ||
| C. | Mg2+ Cl- SO42- | D. | K+ Ca2+ CO32- |
9.pH=2的溶液与下列溶液混合后,所得溶液的pH可能为7的是( )
| A. | pH=0的溶液 | B. | pH=5的溶液 | C. | pH=7的溶液 | D. | pH=11的溶液 |
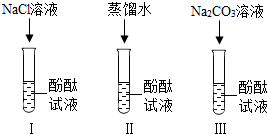 小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请小宁、小明和你一起探究并完成下列问题:
小宁和小明同学学习完酸、碱、盐后发现:碱溶液能使酚酞试液变红,Na2CO3溶液也能使酚酞试液变红.碱溶液使酚酞试液变红,是因为碱在水中解离出OH-,那么Na2CO3溶液中究竟是哪种粒子使酚酞试液变红呢?小宁设计了如图三个实验,请小宁、小明和你一起探究并完成下列问题: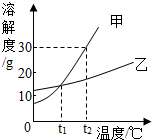 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.