题目内容
化学兴趣小组的同学在实验室发现一瓶保管不当,盛有无色溶液的试剂瓶,且标签破损(如图),其残缺的标签中只剩下“Na”字样.老师告诉他们,这瓶溶液中的溶质可能是氢氧化钠、氯化钠或碳酸钠.同学们很感兴趣,决定对其成分进行探究.【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是 (填字母代号).
A.酸 B.碱 C.盐
【查阅资料】碱性的Na2CO3溶液与中性的CaCl2溶液能发生复分解反应.
【作出猜想】(1)可能是 溶液;(2)可能是Na2CO3溶液;(3)可能是NaCl溶液.
【设计并实验】
| 实验 | 实验操作 | 实验现象 | 实验结论和解释 |
| I | 取样于试管中,向其中滴加几滴 . | 无色溶液变红 | 该溶液不可能是 溶液,理由是 . |
| II | 另取样于试管中,向其中滴加足量的 . | 产生大量气泡 | 该溶液为碳酸钠溶液,有关反应的化学方程式为 . |
【反思】老师指出该结论不严密.理由是:氢氧化钠溶液在空气中敞开放置,发生变质,能产生与实验Ⅰ和Ⅱ相同现象.老师提示,不需另取样,只要在实验Ⅰ后的试管中加入足量CaCl2溶液,若观察到 现象,即可说明该溶液中有氢氧化钠.
【答案】分析:【交流讨论】根据酸、碱、盐的组成特点及标签可见部分,猜测该溶液不可能属于哪类物质的溶液;
【查阅资料】根据提示物质的可能性,对该溶液进行猜想;
【设计并实验】Ⅰ:根据NaCl溶液呈中性,不能使酚酞变色进行解答;Ⅱ:根据酸能和碳酸钠反应生成二氧化碳气体进行解答;
【反思】根据氢氧化钠能和空气中的二氧化碳反应生成碳酸钠而变质,因此要排除碳酸钠碱性对氢氧化钠的干扰碱性分析.
解答:解:【交流讨论】破损标签可见部分为钠元素,可判断该物质由金属元素与根组成,而酸类物质由氢元素与酸根所组成,可判断该物质不可能为酸;故答案为:A;
【查阅资料】除碳酸氢钠外,该溶液可能为氯化钠、碳酸钠或氢氧化钠溶液;故答案为:NaOH;
【设计并实验】Ⅰ:NaCl溶液呈中性,不能使酚酞变色;
Ⅱ:稀盐酸能和碳酸钠反应生成二氧化碳气体,反应的方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【反思】因为氢氧化钠能和空气中的二氧化碳反应生成碳酸钠而变质;若不需另取样,只要在实验Ⅰ后的试管中加入足量CaCl2溶液,氯化钙与碳酸钠完全反应产生碳酸钙沉淀而除去碳酸钠,若观察到产生白色沉淀,且溶液红色不褪去现象,即可说明该溶液中有氢氧化钠.
故答案为:【交流讨论】A;
【作出猜想】NaOH;
【设计并实验】
【反思】:产生白色沉淀,溶液的红色不褪去.
点评:本题综合利用了物质的组成、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.
【查阅资料】根据提示物质的可能性,对该溶液进行猜想;
【设计并实验】Ⅰ:根据NaCl溶液呈中性,不能使酚酞变色进行解答;Ⅱ:根据酸能和碳酸钠反应生成二氧化碳气体进行解答;
【反思】根据氢氧化钠能和空气中的二氧化碳反应生成碳酸钠而变质,因此要排除碳酸钠碱性对氢氧化钠的干扰碱性分析.
解答:解:【交流讨论】破损标签可见部分为钠元素,可判断该物质由金属元素与根组成,而酸类物质由氢元素与酸根所组成,可判断该物质不可能为酸;故答案为:A;
【查阅资料】除碳酸氢钠外,该溶液可能为氯化钠、碳酸钠或氢氧化钠溶液;故答案为:NaOH;
【设计并实验】Ⅰ:NaCl溶液呈中性,不能使酚酞变色;
Ⅱ:稀盐酸能和碳酸钠反应生成二氧化碳气体,反应的方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑;
【反思】因为氢氧化钠能和空气中的二氧化碳反应生成碳酸钠而变质;若不需另取样,只要在实验Ⅰ后的试管中加入足量CaCl2溶液,氯化钙与碳酸钠完全反应产生碳酸钙沉淀而除去碳酸钠,若观察到产生白色沉淀,且溶液红色不褪去现象,即可说明该溶液中有氢氧化钠.
故答案为:【交流讨论】A;
【作出猜想】NaOH;
【设计并实验】
| 实验操作 | 实验结论和解释 |
| 酚酞试液 | NaCl,NaCl溶液不能使酚酞试液变红 |
| 稀盐酸 | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
点评:本题综合利用了物质的组成、溶液的酸碱性及物质的变化规律对未知物质进行鉴别,体现运用化学知识分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.
20、某校化学兴趣小组的同学在阅读资料时发现,18世纪末,法国科学家拉瓦锡曾经做了这样-个实验:让水蒸气通过一根烧红的枪管,生成了一种气体.同学们对这个实验很感兴趣:难道红热的铁能与水蒸气反应?生成的气体又是什么?带着这些疑问,他们设计了如下图所示的装置进行探究.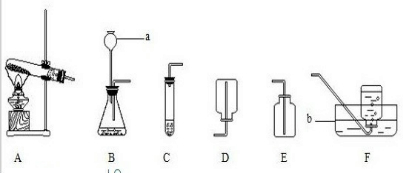
 (2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验:
(2012?太原)某化学兴趣小组的同学在探究Mg、Cu、Fe三种金属的有关性质时进行了如下实验: