题目内容
如图为氯化铵和硫酸钠的溶解度曲线.下列说法中错误的是( )
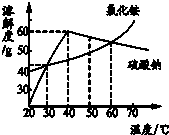

| A、30℃时,氯化铵、硫酸钠的溶解度相等 |
| B、将60℃的硫酸钠饱和溶液降温至30℃,有晶体析出 |
| C、在30℃~70℃范围内,硫酸钠饱和溶液在40℃时溶质质量分数最大 |
| D、40℃时在100g水中加70g硫酸钠,所得溶液质量为170g |
考点:固体溶解度曲线及其作用,晶体和结晶的概念与现象,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:A、溶解度曲线的交点表示该温度下物质的溶解度相等;
B、据硫酸钠的溶解度随温度变化分析解答;
C、据饱和溶液中溶质的质量分数分析解答;
D、据该温度下硫酸钠的溶解度分析解答.
B、据硫酸钠的溶解度随温度变化分析解答;
C、据饱和溶液中溶质的质量分数分析解答;
D、据该温度下硫酸钠的溶解度分析解答.
解答:解:A、溶解度曲线的交点表示该温度下物质的溶解度相等,30℃时,氯化铵、硫酸钠二者的溶解度曲线交于一点,溶解度相等,正确;
B、硫酸钠的溶解度在30℃~40℃范围内,溶解度逐渐变大,在40℃~60℃范围内,溶解度逐渐减小,且60℃时的溶解度大于30℃的溶解度,所以将60℃的硫酸钠饱和溶液降温至30℃,有晶体析出,正确;
C、饱和溶液中溶质的质量分数=
×100%,即溶解度越大质量分数也就越大,在30℃~70℃范围内,硫酸钠溶解度最大,所以饱和溶液在40℃时溶质质量分数最大,正确;
D、40℃硫酸钠的溶解度是60g,即100g水中最多溶解60g的硫酸钠,所以在100g水中加70g硫酸钠,不能完全溶解,所得溶液是160g,故错误;
故选:D.
B、硫酸钠的溶解度在30℃~40℃范围内,溶解度逐渐变大,在40℃~60℃范围内,溶解度逐渐减小,且60℃时的溶解度大于30℃的溶解度,所以将60℃的硫酸钠饱和溶液降温至30℃,有晶体析出,正确;
C、饱和溶液中溶质的质量分数=
| 溶解度 |
| 溶解度+100g |
D、40℃硫酸钠的溶解度是60g,即100g水中最多溶解60g的硫酸钠,所以在100g水中加70g硫酸钠,不能完全溶解,所得溶液是160g,故错误;
故选:D.
点评:明确溶解度概念的含义及溶解度曲线的意义和饱和溶液中溶质的质量分数的计算方法才能正确解答.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
下列各处理浓硫酸方法正确的是( )
| A、不慎把浓硫酸溅到皮肤或衣服上,应用大量的水冲洗 |
| B、在稀释浓硫酸时,一定要把浓硫酸注入水中,不可把水倒入浓硫酸中 |
| C、为了使用方便,浓硫酸可以存放在敞口容器里 |
| D、在10毫升量筒里取9毫升水,再慢慢地向量筒中注入1毫升浓硫酸溶解后配成1:9的硫酸溶液 |
自然界中以现成形式提供的能源称为一级能源,需依靠其他能源间接制得的能源为二级能源.如氢气属高效、无污染的二级能源,是因为自然界中现成的氢气很少.下列叙述正确的是( )
| A、天然气属一级能源 |
| B、煤属二级能源 |
| C、家用电器使用的电能属一级能源 |
| D、风能属二级能源 |
下列实验操作中正确的是( )
| A、量筒用来量取热溶液的体积 |
| B、为了节约火柴,可用燃着的酒精灯点燃另外一盏酒精灯 |
| C、将实验剩余的药品放回原瓶 |
| D、加热试管中的液体,试管口不对着人 |
下列净水的常用方法中属于化学方法的是( )
| A、消毒 | B、吸附沉淀 |
| C、过滤 | D、蒸馏 |
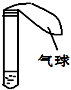 如图所示,试管中盛有某种液体,将气球中的某种固体小心的倒入试管中,能观察到气球变大的一组物质是( )
如图所示,试管中盛有某种液体,将气球中的某种固体小心的倒入试管中,能观察到气球变大的一组物质是( )| A、氯化钠和水 |
| B、铜粉和稀硫酸 |
| C、硝酸铵和水 |
| D、氢氧化钠和水 |
 如图所示:
如图所示: