题目内容
18.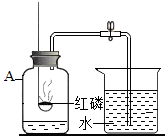 某同学利用如图所示装置来测定空气中氧气的含量.
某同学利用如图所示装置来测定空气中氧气的含量.(1)实验操作主要步骤如下:
①将燃烧匙伸入集气瓶中,并塞紧塞子;
②点燃燃烧匙中的红磷;
③先用弹簧夹夹紧橡皮管;
④燃烧停止后,松开弹簧夹
正确的操作顺序是③②①④;
(2)该实验中红磷稍过量的目的是使集气瓶内的氧气消耗完;
(3)该同学在实验中测定的氧气的体积含量明显低于集气瓶容积的$\frac{1}{5}$请你分析造成这一结果的可能原因是装置漏气(或红磷不足或没有冷却至室温就打开止水夹);
(4)通过该实验可得出关于空气成分的结论是氧气占空气体积的五分之一.
(5)红磷燃烧结束后,集气瓶内剩余气体的主要成分是氮气,请结合本实验推测出氮气的性质:氮气不能与红磷反应,也不能溶于水或与水反应.
分析 本题是测定空气中氧气的含量,我们常用燃烧红磷或白磷的方法,因为磷燃烧生成白色固体五氧化二磷,几乎不占空间,使得内外产生气压差,从而得到正确的结论;保证本实验成功的关键是:①装置气密性好;②红磷要足量;③要冷却至室温再读数.
解答 解:(1)在利用如图所示装置来测定空气中氧气的含量时,先用弹簧夹夹紧橡胶管,然后点燃燃烧匙中的红磷,立即将燃烧匙伸入集气瓶中,并塞紧塞子,等燃烧停止后,冷却至室温时再松开弹簧夹.所以正确的操作顺序是:③②①④.故填:③②①④;
(2)要测定空气中氧气的含量,应将集气瓶内的氧气全部消耗掉,所以该实验中红磷需稍过量的目的是:使集气瓶内的氧气消耗完;故填:使集气瓶内的氧气消耗完;
(3)结果偏小的原因可能有以下几种:①装置气密性不好,在冷却过程中有外界的空气进入瓶中;②红磷量不足,氧气没有完全消耗;③实验没有等到装置冷却至室温就打开止水夹,由于瓶内气体温度偏高,气压偏大,会导致测量结果小等;故填:装置漏气(或红磷不足或没有冷却至室温就打开止水夹);
(4)待红磷熄灭并冷却到室温后,打开弹簧夹,看到的现象:水进入集气瓶约占集气瓶体积的五分之一,说明氧气占空气体积的五分之一;故填:氧气占空气体积的五分之一;
(5)水进入瓶内占五分之一.不再继续进入说明氮气不能与红磷反应,也不能溶于水或与水反应;故填:氮气不能与红磷反应,也不能溶于水或与水反应.
点评 熟记用红磷测定空气里氧气含量的实验原理、操作步骤、实验现象、实验结论和注意事项是解答这类题目的基础.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
6.推理是学习化学的一种方法,以下推理正确的是( )
| A. | 单质中只含有一种元素,因此,只含有一种元素的物质一定是单质 | |
| B. | 碱性溶液的pH大于7,因此,pH大于7的溶液一定是碱性溶液 | |
| C. | 稀有气体原子的最外层电子数为8(氦除外),因此,最外层电子数为8的微粒一定是稀有气体原子 | |
| D. | 中和反应有盐和水生成,因此,有盐和水生成的反应一定是中和反应 |
3.下列属于混合物的是( )
| A. | 冰水混合物 | B. | 氢氧化钙 | C. | 洁净的空气 | D. | 硫酸铜 |
7.下列有关指定容器中水的主要作用的说法,错误的是( )
| 实验 装置 |  硫在氧气中燃烧 |  测定空气中氧气含量 |  铁丝在氧气中燃烧 |  探究燃烧的条件 探究燃烧的条件 |
| 主要作用 | 集气瓶中的水: 吸收反应放出的 热量 | 量筒中的水: 通过水体积的变化得出空气中O2体积分数 | 集气瓶中的水: 冷却溅落的熔融物,防止集气瓶炸裂 | 烧杯中的水: 加热铜片温度, 隔绝空气 |
| 选项 | A | B | C | D |
| A. | A | B. | B | C. | C | D. | D |
8.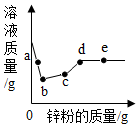 向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )
向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )
 向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )
向一定量硝酸银、硝酸铜和硝酸亚铁的混合溶液中加入锌粉,充分反应后所得溶液的质量与加入锌粉的质量关系如图.下列说法正确的是( )| A. | a点时,溶液中溶质为硝酸锌、硝酸铜、硝酸亚铁 | |
| B. | b点时,所得固体只有银 | |
| C. | c点时,溶液中一定有硝酸锌、硝酸亚铁,可能有硝酸铜 | |
| D. | d点和e点所得固体均为银、铜、铁、锌 |