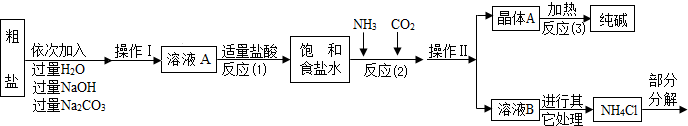
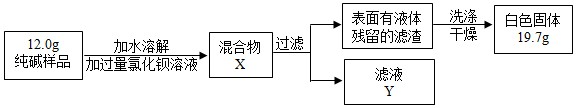
题目内容
氢氧化钠和碳酸钠的混合物, 该样品5.06g放于烧杯中,向其中滴加10%的稀盐酸,所加稀盐酸和产生的气体的质量关系如图所示.
该样品5.06g放于烧杯中,向其中滴加10%的稀盐酸,所加稀盐酸和产生的气体的质量关系如图所示.
(1)求反应完毕后产生二氧化碳的质量?
(2)原固体中氢氧化钠的质量分数是多少?(结果保留一位小数)
解:(1)从图象可以看出,加入36.5克盐酸开始有二氧化碳气体出现,加入43.8克盐酸时二氧化碳的质量达到最大值,所以和碳酸钠反应的盐酸的质量=43.8克-36.5克=7.3克,则氯化氢的质量=7.3克×10%═0.73克.设碳酸钠的质量为X,生成的二氧化碳的质量为Y.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
X 0.73克 Y
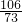 ═
═
得:X=1.06克
 ═
═
得:Y=0.44克
(2)根据(1)的计算可知,样品中氢氧化钠的质量=5.06克-1.06克=4克.
∴样品中氢氧化钠的质量分数= ×100%═79.1%.
×100%═79.1%.
答:反应后生成的二氧化碳的质量为0.44克;样品中氢氧化钠的质量分数为79.1%.
分析:(1)从图象可以看出,加入36.5克盐酸开始有二氧化碳气体出现,加入43.8克盐酸时二氧化碳的质量达到最大值.
(2)写出化学方程式并计算出氢氧化钠和碳酸钠的质量,然后计算出样品中氢氧化钠的质量分数.
点评:掌握化学方程式的计算格式和规范性,本题的关键是知道(43.8-36.5)克盐酸和碳酸钠发生反应.
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 73 44
X 0.73克 Y
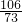 ═
═
得:X=1.06克
 ═
═
得:Y=0.44克
(2)根据(1)的计算可知,样品中氢氧化钠的质量=5.06克-1.06克=4克.
∴样品中氢氧化钠的质量分数=
 ×100%═79.1%.
×100%═79.1%.答:反应后生成的二氧化碳的质量为0.44克;样品中氢氧化钠的质量分数为79.1%.
分析:(1)从图象可以看出,加入36.5克盐酸开始有二氧化碳气体出现,加入43.8克盐酸时二氧化碳的质量达到最大值.
(2)写出化学方程式并计算出氢氧化钠和碳酸钠的质量,然后计算出样品中氢氧化钠的质量分数.
点评:掌握化学方程式的计算格式和规范性,本题的关键是知道(43.8-36.5)克盐酸和碳酸钠发生反应.

练习册系列答案
 天天向上口算本系列答案
天天向上口算本系列答案
相关题目
向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系能用右图所示曲线表示的是( )
| 序号 | 甲 | 乙 |
| A | 铜、锌的混台物 | 稀盐酸 |
| B | 硫酸和硫酸铜的混合溶液 | 氢氧化钠溶液 |
| C | 盐酸和稀硫酸的混合溶液 | 氯化钡溶液 |
| D | 氢氧化钠和碳酸钠的混合溶液 | 稀盐酸 |

向下表的甲物质中逐滴加入相应的乙溶液至过量,反应过程中生成气体或沉淀的质量与加入乙的质量关系能用右图所示曲线表示的是( )
| 序号 | 甲 | 乙 |
| A | 铜、锌的混台物 | 稀盐酸 |
| B | 硫酸和硫酸铜的混合溶液 | 氢氧化钠溶液 |
| C | 盐酸和稀硫酸的混合溶液 | 氯化钡溶液 |
| D | 氢氧化钠和碳酸钠的混合溶液 | 稀盐酸 |