题目内容
“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用的工艺和技术。
(1)最近有科学家提出“绿色自由”构想:把CO2含量高的气体吹入饱和K2CO3溶液中,生成KHCO3,然后利用KHCO3受热易分解的性质,再把CO2提取出来,经化学反应使之变为甲醇(CH3OH)和水。“绿色自由”构想的技术流程如下图:

(注:分解池内的反应条件是加热;合成塔内的反应条件为300 ℃、200 kPa和催化剂)
①分解池内反应的化学方程式为____________________________________________;
②合成塔内反应的化学方程式为__________________________________________;
③X溶液可循环利用,溶质是________(填写化学式)。
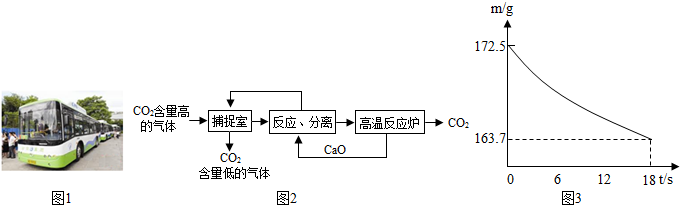
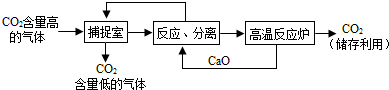
(2)实际生产中,经常利用NaOH溶液来“捕捉”CO2,流程如下图(部分条件及物质未标出)。

①捕捉室内反应的化学方程式为___________________________________________;
②“反应分离”发生反应的化学方程式为________________,__________________;
③该生产过程中,涉及的物质属于碱的是________(填写化学式)。
答案:(1)①2KHCO3△,K2CO3+H2O+CO2↑
②3H2+CO2 CH3OH+H2O
CH3OH+H2O
③K2CO3
(2)①CO2+2NaOH===Na2CO3+H2O
②CaO+H2O===Ca(OH)2 Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
③Ca(OH)2、NaOH
解析:(1)由图示和题中信息可知:①KHCO3受热分解生成K2CO3、H2O和CO2;②CO2和H2在300 ℃、200 kPa和催化剂的条件下生成CH3OH和水;③可循环利用的是K2CO3溶液,溶质是K2CO3。
(2)由流程图可知:①CO2与NaOH反应生成Na2CO3和H2O;②CaO和H2O生成Ca(OH)2,Ca(OH)2和Na2CO3反应生成CaCO3和NaOH;③该生产过程中,Ca(OH)2、NaOH属于碱。