题目内容
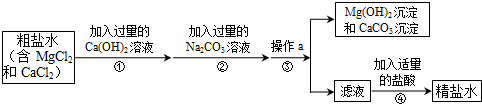
8.请根据如图所示的实验过程和提供的数据(步骤②产生的气体全部逸出),回答下列问题:
(1)实验中生成的气体的质量为4.4g.
(2)计算原混合物样品中CaCl2的质量分数(写出计算过程).
分析 (1)根据图中信息可以知道,反应前加入的物质的总质量为:12g+100g+100g=212g,而反应后剩余物质的总质量为207.6g,根据质量守恒定律可以知道物质减少的质量为生成二氧化碳的质量;
(2)根据二氧化碳的质量结合化学方程式可以求算出碳酸钙的质量,进而可以求出氯化钙的质量.
解答 解:(1)反应中生成CO2的质量为:12g+100g+100g-207.6g=4.4g;答案:(1)4.4g
(2)解:设原混合物中 CaCO3的质量为x
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 44
x 4.4g
$\frac{100}{44}=\frac{x}{4.4g}$,
x=10g
原混合物样品中CaCl2的质量分数为:12g-10g/12g×100%=16.7%
答:原混合物样品中CaCl2的质量为16.7%.
点评 要想解答好这类题目,首先,要理解和熟记根据化学反应方程式的计算步骤和格式,以及与之相关的知识等.然后,根据所给的问题情景或图表信息等,结合所学的相关知识和技能,细致地分析题意(或图表信息)等各种信息资源,并细心地探究、推理后,按照题目要求进行认真地选择或解答即可.

练习册系列答案
相关题目
19.下列物质中能与澄清石灰水反应,但反应若不加指示剂则无明显现象的是( )
| A. | 氯化铁溶液 | B. | 碳酸钠溶液 | C. | 稀盐酸 | D. | 硝酸溶液 |
16.下列说法正确的是( )
| A. | 化学变化就是化学反应 | |
| B. | 物理变化过程中一定同时发生化学变化 | |
| C. | 化学变化过程中不一定同时发生物理变化 | |
| D. | 蜡烛燃烧的过程只发生化学变化而不发生物理变化 |
3.用托盘天平称量一盛有粉剂的烧杯,若左盘上放有20g砝码,当天平指针为零,游码位置在2.2g时,烧杯和粉剂的质量为( )
| A. | 22.2 g | B. | 20 g | C. | 17.8 g | D. | 2.2 g |
13.化学影响着社会的发展和人们的生活质量,以下说法正确的是( )
| A. | 焚烧废旧塑料可以解决“白色污染”问题 | |
| B. | 为了加强食品的色、香、味,可以大量使用添加剂 | |
| C. | 糖类和油脂在人体内经氧化放出能量,为机体活动和维持恒定体温提供能量 | |
| D. | 网状结构的高分子材料具有热塑性 |
20.下列各组气体混合,遇明火可能会发生爆炸的( )
| A. | N2和O2 | B. | H2和O2 | C. | CO2和空气 | D. | CO和N2 |
17.(1)在研究金属性质时,某小组同学进行了如下实验探究:将一定量铁粉加入到硫酸锌和硫酸铜的混合溶液中,充分反应后过滤,然后对滤纸上的物质进行分析和实验.
【提出问题】滤纸上的物质是什么?
【做出猜想】甲认为只有铜;乙认为是铜和铁的混合物;丙认为是铜、铁、锌的混合物.
【交流讨论】大家一致认为丙的猜想不合理,其理由是铁排在锌的后边,不能置换出锌.
【实验与结论】同学们通过实验确定了滤纸上物质的成分.请填写下列空白.
(4)钢铁是人类生活和生产中非常重要的材料.
①工业炼铁的反应过程如图所示.其中焦炭的作用是为了生成还原剂一氧化碳;属于化合反应的是反应Ⅰ和反应Ⅱ.

②在工业冶炼中要得到224t铁,理论上需要含Fe2O3 80%的赤铁矿石的质量是多少?
【提出问题】滤纸上的物质是什么?
【做出猜想】甲认为只有铜;乙认为是铜和铁的混合物;丙认为是铜、铁、锌的混合物.
【交流讨论】大家一致认为丙的猜想不合理,其理由是铁排在锌的后边,不能置换出锌.
【实验与结论】同学们通过实验确定了滤纸上物质的成分.请填写下列空白.
| 实验步骤 | 现象和结论 | 有关反应的化学方程式 |
| 取少量滤纸上剩余的物质置于试管中,加入适量的溶液 稀盐酸 | 有气泡冒出,证明是铜和铁的混合物 | Fe+2HCl=FeCl2+H2↑ |
①工业炼铁的反应过程如图所示.其中焦炭的作用是为了生成还原剂一氧化碳;属于化合反应的是反应Ⅰ和反应Ⅱ.

②在工业冶炼中要得到224t铁,理论上需要含Fe2O3 80%的赤铁矿石的质量是多少?