题目内容
日常生活中人们广泛使用金属材料.
(1)下列关于金属材料的说法正确的是 (填字母序号).
A.铝是人类最早利用的金属材料
B.铜是目前世界年产量最高的金属
C.大多数金属元素在自然界中以单质形式存在
D.日常使用的金属材料大多数是合金
(2)选择铸造硬币的材料不需要考虑的因素是 (填字母序号).
A.金属的导电性 B.金属的耐腐蚀性
C.金属的硬度 D.金属价格与硬币面值的吻合度
(3)以上硬币涉及到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:
Ni+H2SO4═NiSO4+H2↑ Fe+NiCl2═Ni+FeCl2
这两个反应的基本类型都是 .四种金属活动性由强到弱的顺序为 (用元素符号表示).
(4)工业炼铁可以把赤铁矿(主要成分为Fe2O3)在高炉里和CO反应,生成单质铁,该反应的化学方程式是 ;
①氧化铁(Fe2O3)的相对分子质量是 ;
②2000t含氧化铁84%的赤铁矿中理论上可炼得含铁98%的生铁 t.
(1)下列关于金属材料的说法正确的是
A.铝是人类最早利用的金属材料
B.铜是目前世界年产量最高的金属
C.大多数金属元素在自然界中以单质形式存在
D.日常使用的金属材料大多数是合金
(2)选择铸造硬币的材料不需要考虑的因素是
A.金属的导电性 B.金属的耐腐蚀性
C.金属的硬度 D.金属价格与硬币面值的吻合度
(3)以上硬币涉及到Fe、Cu、Al、Ni(镍),已知Ni能够发生如下反应:
Ni+H2SO4═NiSO4+H2↑ Fe+NiCl2═Ni+FeCl2
这两个反应的基本类型都是
(4)工业炼铁可以把赤铁矿(主要成分为Fe2O3)在高炉里和CO反应,生成单质铁,该反应的化学方程式是
①氧化铁(Fe2O3)的相对分子质量是
②2000t含氧化铁84%的赤铁矿中理论上可炼得含铁98%的生铁
考点:金属材料及其应用,金属的物理性质及用途,合金与合金的性质,金属活动性顺序及其应用,金属元素的存在及常见的金属矿物,铁的冶炼,含杂质物质的化学反应的有关计算,相对分子质量的概念及其计算
专题:金属与金属材料
分析:(1)根据金属的性质进行解答;
(2)根据选择铸造硬币的材料不需要考虑的因素是导电性进行解答;
(3)根据金属活动性顺序角度思考进行解答;
(4)根据赤铁矿的主要成分为氧化铁,则CO和氧化铁反应生成铁和二氧化碳来书写化学反应方程式;以及将氧化铁的质量代入化学反应方程式来计算铁的质量.
(2)根据选择铸造硬币的材料不需要考虑的因素是导电性进行解答;
(3)根据金属活动性顺序角度思考进行解答;
(4)根据赤铁矿的主要成分为氧化铁,则CO和氧化铁反应生成铁和二氧化碳来书写化学反应方程式;以及将氧化铁的质量代入化学反应方程式来计算铁的质量.
解答:解:(1)A.铜是人类最早利用的金属材料,故A错误;
B.铁是目前世界年产量最高的金属,故B错误;
C.大多数金属元素在自然界中以化合物形式存在,故C错误;
D.日常使用的金属材料大多数是合金,故D正确;故选:D;
(2)选择铸造硬币的材料不需要考虑的因素是导电性,而应该考虑金属的耐腐蚀性、金属的硬度、金属价格与硬币面值的吻合度,故选:A;
(3)在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,这两个反应都是一种单质和一种化合物生成一种单质和一种化合物的反应,属于置换反应;
Ni+H2SO4═NiSO4+H2↑,说明Ni>H;
Fe+NiCl2═Ni+FeCl2,说明Fe>Ni;
故这四种金属的活动性顺序为:Al>Fe>Ni>Cu;
故填:置换反应;Al>Fe>Ni>Cu;
(4)根据氧化铁和CO反应生成二氧化碳和铁,则反应的化学方程式为Fe2O3+3CO
3CO2+2Fe,故答案为:Fe2O3+3CO
3CO2+2Fe;
(2)①氧化铁(Fe2O3)的相对分子质量=56×2+16×3=160;故填:160;
②由2000t含氧化铁84%的赤铁矿,则氧化铁的质量为2000t×84%=1680t.
设可炼得含铁98%的生铁x,则
Fe2O3+3CO
3CO2+2Fe
160 112
1680t x×98%
=
解得x=1200t,
答:即可炼得含铁98%的生铁1200t.
故答案为:1200.
B.铁是目前世界年产量最高的金属,故B错误;
C.大多数金属元素在自然界中以化合物形式存在,故C错误;
D.日常使用的金属材料大多数是合金,故D正确;故选:D;
(2)选择铸造硬币的材料不需要考虑的因素是导电性,而应该考虑金属的耐腐蚀性、金属的硬度、金属价格与硬币面值的吻合度,故选:A;
(3)在金属活动性顺序中,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,这两个反应都是一种单质和一种化合物生成一种单质和一种化合物的反应,属于置换反应;
Ni+H2SO4═NiSO4+H2↑,说明Ni>H;
Fe+NiCl2═Ni+FeCl2,说明Fe>Ni;
故这四种金属的活动性顺序为:Al>Fe>Ni>Cu;
故填:置换反应;Al>Fe>Ni>Cu;
(4)根据氧化铁和CO反应生成二氧化碳和铁,则反应的化学方程式为Fe2O3+3CO
| ||
| ||
(2)①氧化铁(Fe2O3)的相对分子质量=56×2+16×3=160;故填:160;
②由2000t含氧化铁84%的赤铁矿,则氧化铁的质量为2000t×84%=1680t.
设可炼得含铁98%的生铁x,则
Fe2O3+3CO
| ||
160 112
1680t x×98%
| 160 |
| 1680t |
| 112 |
| x×98% |
解得x=1200t,
答:即可炼得含铁98%的生铁1200t.
故答案为:1200.
点评:本题主要考察了金属的性质、用途和金属活动性顺序以及金属防锈的有关知识,比较简单.

练习册系列答案
 同步练习河南大学出版社系列答案
同步练习河南大学出版社系列答案 同步练习西南大学出版社系列答案
同步练习西南大学出版社系列答案 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案
相关题目
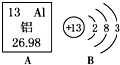 如图A是某元素在元素周期表中的相关信息,B是其原子结构示意图.
如图A是某元素在元素周期表中的相关信息,B是其原子结构示意图. 在实验室可用如图装置制取蒸馏水.回答下列问题:
在实验室可用如图装置制取蒸馏水.回答下列问题: