题目内容
在托盘天平两边各放一只烧杯,调节至平衡,再向两只烧杯中各注入相同质量、相同质量分数的稀硫酸,然后分别投入相同质量的锌粒和镁带,待反应停止后,天平指针指向分度盘的中间,下列可能出现的情况是
- A.锌粒和镁带都有剩余
- B.锌粒完全反应镁带剩余
- C.镁带完全反应锌粒剩余
- D.锌粒和镁带都完全反应
AB
分析:反应停止后,天平指针在中间,反应前烧杯中加入的质量相等,则产生的氢气相等,天平才平衡.根据氢气质量相等分析.
解答:A、锌粒和镁带都有剩余,说明酸完全反应,酸的质量相等,故产生氢气质量相等,正确;
B、由化学方程式Zn+H2SO4 ═ZnSO4+H2↑和Mg+H2SO4 ═MgSO4+H2↑可以看出,等质量的硫酸消耗掉锌的质量大于镁的质量,故当锌粒完全反应镁一定有剩余,此时酸完全反应,产生氢气质量相等,故正确;
C、由化学方程式Zn+H2SO4 ═ZnSO4+H2↑和Mg+H2SO4 ═MgSO4+H2↑可以看出,等质量的硫酸消耗掉锌的质量大于镁的质量,当镁带完全反应时锌粒一定没有剩余,故错误;
D、由化学方程式Zn+H2SO4 ═ZnSO4+H2↑和Mg+H2SO4 ═MgSO4+H2↑可以看出,等质量的锌粒和镁带完全反应时,生成氢气的质量一定不相等,故D错误;
故选AB
点评:解答本题的关键是根据天平平衡分析产生氢气质量相等.
分析:反应停止后,天平指针在中间,反应前烧杯中加入的质量相等,则产生的氢气相等,天平才平衡.根据氢气质量相等分析.
解答:A、锌粒和镁带都有剩余,说明酸完全反应,酸的质量相等,故产生氢气质量相等,正确;
B、由化学方程式Zn+H2SO4 ═ZnSO4+H2↑和Mg+H2SO4 ═MgSO4+H2↑可以看出,等质量的硫酸消耗掉锌的质量大于镁的质量,故当锌粒完全反应镁一定有剩余,此时酸完全反应,产生氢气质量相等,故正确;
C、由化学方程式Zn+H2SO4 ═ZnSO4+H2↑和Mg+H2SO4 ═MgSO4+H2↑可以看出,等质量的硫酸消耗掉锌的质量大于镁的质量,当镁带完全反应时锌粒一定没有剩余,故错误;
D、由化学方程式Zn+H2SO4 ═ZnSO4+H2↑和Mg+H2SO4 ═MgSO4+H2↑可以看出,等质量的锌粒和镁带完全反应时,生成氢气的质量一定不相等,故D错误;
故选AB
点评:解答本题的关键是根据天平平衡分析产生氢气质量相等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
在托盘天平两边各放一只烧杯,调节至平衡.在两烧杯中分别注入等质量等浓度且足量的稀硫酸,在左烧杯中投入少量的锌粒,在右烧杯中投入相同质量的镁条,锌粒和镁条完全溶解后,天平的指针( )
| A、偏左 | B、偏右 | C、指向中间 | D、无法判断 |

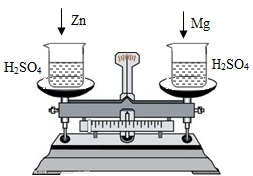 在托盘天平两边各放一只烧杯,调节至平衡,再向两只烧杯中各注入相同质量相同质量分数的稀硫酸,然后按下图所示分别投入相同质量的锌和镁带,待反应停止后,天平指针的可能指向是( )
在托盘天平两边各放一只烧杯,调节至平衡,再向两只烧杯中各注入相同质量相同质量分数的稀硫酸,然后按下图所示分别投入相同质量的锌和镁带,待反应停止后,天平指针的可能指向是( ) 在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的Fe和金属A.有气体产生时,天平指针慢慢向左偏转(如图1):指针偏转到一定角度后,又慢慢向右偏转;反应结束后,天平指针指向右端(如图2).则天平右端加入金属A可能是( )
在托盘天平两边各放一只烧杯,调节至平衡.在两只烧杯里注入相同质量、相同质量分数的足量稀盐酸,然后分别向左右两端烧杯中加入质量相等的Fe和金属A.有气体产生时,天平指针慢慢向左偏转(如图1):指针偏转到一定角度后,又慢慢向右偏转;反应结束后,天平指针指向右端(如图2).则天平右端加入金属A可能是( )