题目内容
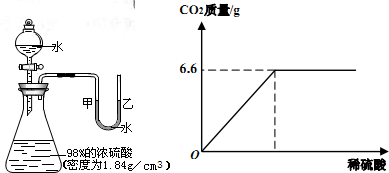
某同学从制碱厂带回一瓶废弃的纯碱样品,决定测定其中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质).她取样品30g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如右图所示,求:(计算结果用百分数表示,保留到小数点后一位数字.)样品中碳酸钠的质量分数.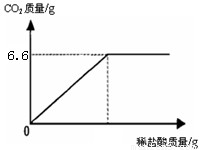
【答案】分析:根据生成CO2气体的质量与滴加稀盐酸的质量关系图可知,恰好完全反应时,生成二氧化碳气体的质量为6.6g,根据二氧化碳气体的质量可计算参加反应的碳酸钠的质量,进而计算出样品中碳酸钠的质量分数.
解答:解:设样品中碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 6.6g
 x=15.9g
x=15.9g
样品中碳酸钠的质量分数为: ×100%=53%.
×100%=53%.
答:样品中碳酸钠的质量分数为53%.
点评:本题难度不是很大,理解题意、抓住“三点一趋势”(起点、拐点、终点和图象的变化趋势)、分析图象中所给数据的含义、正确的运用有关数据解决问题是解答此类题目的关键所在.
解答:解:设样品中碳酸钠的质量为x.
Na2CO3+2HCl=2NaCl+CO2↑+H2O
106 44
x 6.6g
 x=15.9g
x=15.9g 样品中碳酸钠的质量分数为:
 ×100%=53%.
×100%=53%.答:样品中碳酸钠的质量分数为53%.
点评:本题难度不是很大,理解题意、抓住“三点一趋势”(起点、拐点、终点和图象的变化趋势)、分析图象中所给数据的含义、正确的运用有关数据解决问题是解答此类题目的关键所在.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
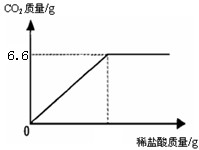 某同学从制碱厂带回一瓶废弃的纯碱样品,决定测定其中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质).她取样品30g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如右图所示,求:(计算结果用百分数表示,保留到小数点后一位数字.)样品中碳酸钠的质量分数.
某同学从制碱厂带回一瓶废弃的纯碱样品,决定测定其中碳酸钠的质量分数(假设该样品中只含有氯化钠一种杂质).她取样品30g逐滴加入稀盐酸,生成CO2气体的质量与滴加稀盐酸的质量关系如右图所示,求:(计算结果用百分数表示,保留到小数点后一位数字.)样品中碳酸钠的质量分数.