题目内容
【题目】(1)良好的生态环境、饮食习惯可以提升生活质量。
①近期雾霾天气影响了很多人的生活。导致雾霾形成的主要污染物是______(填字母)。
a.SO2 b.NO2 c.PM2.5
②燃料不完全燃烧会对环境有污染。46g酒精在88g氧气中恰好完全反应,生成66g二氧化碳54g水以及第三种物质。请根据数据得出第三种物质的化学式______,并写出该反应的化学方程式______。
③垃圾无害化处理有利于保护环境。下列有关生活垃圾的处理合理的是_______。
a.用厨余垃圾生产沼气 b.废旧塑料露天焚烧 c.废旧电池就地填埋
④新鲜蔬菜富含维生素C,蔬菜生吃比熟吃时维生素C的损失小,由此推测维生素C可能具有的化学性质有______。
(2)材料的不断发展可以促进社会进步。
①铝制品不易生锈的原因是______。
②氮化硅(Si3N4)是一种新型高温材料,由高纯硅和氮气在1300℃时反应制的。化学方程式为______。
(3)防止食品变质,常在包装袋中放一袋干燥剂。
①写出干燥剂氧化钙吸水的化学方程式______。
②取24.8g长期暴露在空气中的氧化钙样品,加入足量的盐酸,产生CO2 4.4 g,再向剩余溶液中加入足量的Na2CO3溶液,充分反应后,过滤得到沉淀质量为30g。根据上述数据判断,样品固体中碳酸钙的质量为___g,____(填“存在”或“不存在”)氧化钙。
【答案】 c CO 4C2H6O+11O2![]() 6CO2+12H2O+2CO a 受热性质会变化 铝在空气中易与空气中的氧气反应生成致密的氧化铝膜 3Si+2N2
6CO2+12H2O+2CO a 受热性质会变化 铝在空气中易与空气中的氧气反应生成致密的氧化铝膜 3Si+2N2![]() Si3N4 CaO+H2O=Ca(OH)2 10 不存在
Si3N4 CaO+H2O=Ca(OH)2 10 不存在
【解析】(1)①导致雾霾形成的主要污染物是PM2.5,故选c。②酒精不充分燃烧有一氧化碳气体生成,根据质量守恒定律,生成一氧化碳的质量是:46g+88g-66g-54g=14g,C2H6O+O2 ![]() CO2+H2O+CO ,各物质的分子个数比为:
CO2+H2O+CO ,各物质的分子个数比为:![]() :
:![]() :
:![]() :
:![]() :
:![]() =4:11:6:12:2,所以反应的化学方程式为:4C2H6O+11O2
=4:11:6:12:2,所以反应的化学方程式为:4C2H6O+11O2![]() 6CO2+12H2O+2CO ③a.用厨余垃圾生产沼气,变废为宝,正确;b.废旧塑料露天焚烧,产生有害气体,错误;c.废旧电池就地填埋会对水土造成严重污染,错误。故选a。④新鲜蔬菜富含维生素C,蔬菜生吃比熟吃时维生素C的损失小,由此推测维生素C可能具有的化学性质有受热性质会变化。(2)①铝制品不易生锈的原因是,铝在空气中易与空气中的氧气反应生成致密的氧化铝膜,阻止铝进一步氧化。②根据题意反应的化学方程式为:3Si+2N2
6CO2+12H2O+2CO ③a.用厨余垃圾生产沼气,变废为宝,正确;b.废旧塑料露天焚烧,产生有害气体,错误;c.废旧电池就地填埋会对水土造成严重污染,错误。故选a。④新鲜蔬菜富含维生素C,蔬菜生吃比熟吃时维生素C的损失小,由此推测维生素C可能具有的化学性质有受热性质会变化。(2)①铝制品不易生锈的原因是,铝在空气中易与空气中的氧气反应生成致密的氧化铝膜,阻止铝进一步氧化。②根据题意反应的化学方程式为:3Si+2N2![]() Si3N4(3)①氧化钙能与水反应生成氢氧化钙。②产生的4.4gCO2是碳酸钙与稀盐酸反应产生的,设样品固体中碳酸钙的质量为x。
Si3N4(3)①氧化钙能与水反应生成氢氧化钙。②产生的4.4gCO2是碳酸钙与稀盐酸反应产生的,设样品固体中碳酸钙的质量为x。
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
100 44
x 4.4g
![]() =
=![]() ,解得x=10g
,解得x=10g
则样品中其它物质的质量为:24.8g-10g=14.8g,由其它物质与碳酸钠反应生成沉淀的质量为:30g-10g=20g,设参加反应的氢氧化钙的质量是y。
根据化学方程式:Na2CO3 + Ca(OH)2 == CaCO3↓+ 2NaOH,
74 100
y 20g
![]()
![]() =
=![]() ,解得y=14.8g,所以样品固体中不存在氧化钙。
,解得y=14.8g,所以样品固体中不存在氧化钙。

【题目】已知硝酸钾在不同温度下的溶解度如下表:
温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度/g | 32 | 46 | 64 | 85.5 | 110 | 138 | 170 |
甲是80℃含有100 g水的KNO3溶液,操作过程如下图所示。以下分析错误的是
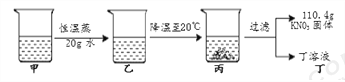
A. 甲、乙、丙、丁四种溶液中,饱和溶液只有2种
B. 甲到乙的过程中,溶质质量没有改变
C. 甲溶液中,溶剂与溶质的质量比为25: 34
D. 甲溶液冷却时,开始析出固体的温度在60℃~70℃之间