题目内容
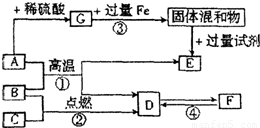
如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体,B、C、D通常均为无色气体,F为一种不含氢元素的钠盐,G溶液为蓝色,相互转化关系如图.请根据上图回答下列问题:(1)物质A、F的化学式分别为 、 .
(2)反应③的化学方程式为 .
(3)③中获得固体混合物的操作名称是 ,其中玻璃棒的作用是 ;该固体混合物中所含物质的化学式是 ,要从中分离出E物质,所加的过量试剂的名称是 .
(4)所有转化过程中没有涉及的化学反应基本类型是 反应.
【答案】分析:G为蓝色溶液属于铜离子溶液,A与硫酸反应生成G,所以G是硫酸铜,A为含铜的黑色固体,所以是氧化铜,E由氧化铜被还原制得,且属于红色固体单质,所以E是铜;F为不含有氢元素的钠盐,且与D能相互转化,D还是氧化铜被还原后的产物,再根据三大还原剂进行考虑,D属于气体能制得碳酸钠,所以D是二氧化碳,A与B反应生成铜和二氧化碳;B和C二氧化碳,说明C是助燃性的氧气;再根据方程式的写法和物质的分离方法回答本题.
解答:解:(1)铜离子溶液是蓝色,G为蓝色溶液所以属于铜离子溶液,A与硫酸反应生成G(属于置换反应),所以G是硫酸铜,A为含铜的黑色固体,所以是氧化铜,E由氧化铜被还原后制得,且属于红色固体单质,所以E是铜;F为不含有氢元素的钠盐,D与F能相互转化,D是还原性物质与助燃性的氧气生成的水或二氧化碳(属于化合反应),只有二氧化碳能与碳酸钠相互转化,所以D是二氧化碳,F是碳酸钠(其中碳酸钠和酸反应属于复分解反应);
(2)因为G是硫酸铜,故可以和铁发生置换反应:Fe+CuSO4═FeSO4+Cu;
(3)将固体和液体分离采用过滤法,其中玻璃棒起到引流作用,固体混合物中有生成的铜和过量的铁,要将铜分离出来,可以加入酸与铁反应或采用强金属置换弱金属的方法;故答案为:稀盐酸(或稀硫酸)或含铜离子的盐溶液;
(4)发生的反应类型有上述的置换反应、复分解反应、化合反应,没有分解反应.
故答案为:(1)CuO Na2CO3 (2)Fe+CuSO4═FeSO4+Cu (3)过滤 引流 Fe和Cu 稀盐酸(或稀硫酸)或含铜离子的盐溶液 (4)分解.
点评:解答本题关键是找出突破口,G为蓝色溶液是铜离子溶液,A为黑色固体与硫酸反应生成G,所以G是硫酸铜,还需要知道黑色固体有:铁、氧化铜、二氧化锰、四氧化三铁、碳等物质,A为含铜的黑色固体,所以是氧化铜,再进一步进行分析即可;根据所提供的可能存在的物质的性质,结合实验现象逐渐确定物质,是解决此类实验推断题的最基本方法.
解答:解:(1)铜离子溶液是蓝色,G为蓝色溶液所以属于铜离子溶液,A与硫酸反应生成G(属于置换反应),所以G是硫酸铜,A为含铜的黑色固体,所以是氧化铜,E由氧化铜被还原后制得,且属于红色固体单质,所以E是铜;F为不含有氢元素的钠盐,D与F能相互转化,D是还原性物质与助燃性的氧气生成的水或二氧化碳(属于化合反应),只有二氧化碳能与碳酸钠相互转化,所以D是二氧化碳,F是碳酸钠(其中碳酸钠和酸反应属于复分解反应);
(2)因为G是硫酸铜,故可以和铁发生置换反应:Fe+CuSO4═FeSO4+Cu;
(3)将固体和液体分离采用过滤法,其中玻璃棒起到引流作用,固体混合物中有生成的铜和过量的铁,要将铜分离出来,可以加入酸与铁反应或采用强金属置换弱金属的方法;故答案为:稀盐酸(或稀硫酸)或含铜离子的盐溶液;
(4)发生的反应类型有上述的置换反应、复分解反应、化合反应,没有分解反应.
故答案为:(1)CuO Na2CO3 (2)Fe+CuSO4═FeSO4+Cu (3)过滤 引流 Fe和Cu 稀盐酸(或稀硫酸)或含铜离子的盐溶液 (4)分解.
点评:解答本题关键是找出突破口,G为蓝色溶液是铜离子溶液,A为黑色固体与硫酸反应生成G,所以G是硫酸铜,还需要知道黑色固体有:铁、氧化铜、二氧化锰、四氧化三铁、碳等物质,A为含铜的黑色固体,所以是氧化铜,再进一步进行分析即可;根据所提供的可能存在的物质的性质,结合实验现象逐渐确定物质,是解决此类实验推断题的最基本方法.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目



 如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据图回答下列问题:
如图A~G是初中化学常见的物质,其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据图回答下列问题: 如图A~G是初中化学常见的物质:其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据下图回答下列问题:
如图A~G是初中化学常见的物质:其中A为黑色固体,E为红色固体单质,B、C、D均为无色气体,F为石灰石的主要成分,G为蓝色溶液,请根据下图回答下列问题: