题目内容
由Mg(OH)2和MgO组成的混合物,测得其中镁元素的质量分数为48%.取该混合物10g,与90g稀硫酸恰好完全反应,所得溶液中溶质的质量分数为( )
| A、12% | B、24% |
| C、36% | D、48% |
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据镁元素的质量分数可计算镁元素的质量,利用反应后的溶质为硫酸镁,根据镁原子守恒来计算硫酸镁的质量,混合物与酸的质量和为溶液质量,最后计算溶质的质量分数.
解答:解:混合物中镁元素的质量为10g×48%=4.8g,
设恰好完全反应后溶液中硫酸镁的质量为xg,
由镁元素守恒可知,
Mg~MgSO4
24 120
4.8g x
=
x=24g
反应后溶液质量为10g+90g=100g
所得溶液中溶质的质量分数为:
×100%=24%
故选B.
设恰好完全反应后溶液中硫酸镁的质量为xg,
由镁元素守恒可知,
Mg~MgSO4
24 120
4.8g x
| 24 |
| 4.8g |
| 120 |
| x |
x=24g
反应后溶液质量为10g+90g=100g
所得溶液中溶质的质量分数为:
| 24g |
| 100g |
故选B.
点评:本题考查溶液中溶质质量分数的计算,学生应能利用元素守恒的方法来计算溶质的质量是解答中的关键,不可盲目利用化学方程式来计算溶质质量.

练习册系列答案
 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目
下列物质的用途利用其化学性质的是( )
| A、石墨作铅笔芯 |
| B、金刚石作钻头 |
| C、用铜丝作导线 |
| D、天然气作燃料 |
已知某两种物质在光照条件下能发生化学反应,其微观示意图如图所示,则下列说法正确的是( )
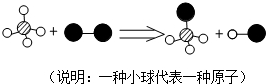

| A、图示中共有4种分子 |
| B、该反应属于化合反应 |
| C、图示中的反应物都是单质 |
| D、该图示不符合质量守恒定律 |
下列能量的转化过程中,属于化学变化的是( )
| A、太阳能热水器提供热水 |
| B、电热器取暖 |
| C、燃煤火力发电 |
| D、水力发电 |
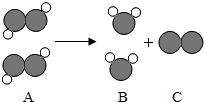 若用○和●表示不同元素的原子,如图为A在一定条件下生成B和C,反应前后分子种类变化的微观示意图如图所示.
若用○和●表示不同元素的原子,如图为A在一定条件下生成B和C,反应前后分子种类变化的微观示意图如图所示.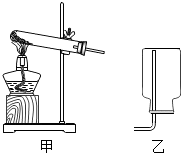 如图是实验室常见的制取和收集气体的装置,在O2、H2、CO2三种气体中,甲装置可以用来制取
如图是实验室常见的制取和收集气体的装置,在O2、H2、CO2三种气体中,甲装置可以用来制取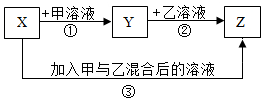 X、Y、Z分别是三种不同的酸溶液.其中X和Z是含氧酸溶液.三者之间有如下的转化关系:
X、Y、Z分别是三种不同的酸溶液.其中X和Z是含氧酸溶液.三者之间有如下的转化关系: