题目内容
1.对于mg硫和ng氧气燃烧生成二氧化硫的质量,最合理的是( )| A. | 等于(m+n)g | B. | 小于(m+n)g | C. | 大于(m+n) g | D. | 不大于(m+n ) g |
分析 由题意“将mg硫放在ng氧气中燃烧时”,根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,则可知所生成二氧化硫质量:小于或等于(m+n)g.
解答 解:由题意“将mg硫放在ng氧气中燃烧时”,根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和,则可知所生成二氧化硫质量:二者正好完全反应,则所生成二氧化硫质量:等于(m+n)g;如果二者中有一种剩余,则小于(m+n)g;等于或小于(m+n)g即不大于(m+n)g.
故选D.
点评 反应物的物质质量比若与根据化学方程式所计算的反应物间各物质质量比相符,则反应物恰好完全反应,否则会有物质剩余而未全部参加反应.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
11.实验设计是化学实验的重要环节.请根据下列实验要求回答相关问题:
【活动与探究一】用对比实验方法探究二氧化碳的性质.
(1)实验一中振荡3个矿泉水塑料瓶,观察到塑料瓶变瘪的程度为A>B>C,其中变浑浊的瓶内发生反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O;对比A瓶与C(填“B”或“C”)瓶的实验现象,可证明CO2能与NaOH发生反应.
(2)实验二观察到C装置中发生的现象是干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色,结论是CO2+H2O=H2CO3(用化学方程式表示.
【活动与探究一】用对比实验方法探究二氧化碳的性质.
| 实验一 | 实验二 |
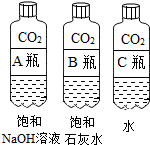 |  |
(2)实验二观察到C装置中发生的现象是干燥的石蕊试纸无变化,湿润的蓝色石蕊试纸变红色,结论是CO2+H2O=H2CO3(用化学方程式表示.
12.除去下列各组物质中少量的杂质,所用试剂或方法正确的是( )
| 物质 | 杂质 | 除杂所用试剂或方法 | |
| A | CO2 | CO | 足量O2,点燃 |
| B | Fe | Cu | 加入稀盐酸,过滤、洗涤、干燥 |
| C | N2 | O2 | 通过灼热的铜网 |
| D | Cu | Fe2O3 | 通入足量CO |
| A. | A | B. | B | C. | C | D. | D |
16.下列物质的用途,只利用了其物理性质的是( )
| A. | 用氦气灌充探空气球 | B. | 用氧气做火箭的助燃剂 | ||
| C. | 用稀有气体制作霓虹灯 | D. | 利用镁粉制作照明弹 |
13.除去二氧化碳中少量一氧化碳气体,可将混合气体( )
| A. | 点燃 | B. | 通过灼热的碳层 | ||
| C. | 通入足量澄清石灰水 | D. | 通过灼热的氧化铜 |
10. 一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示.下列关于该反应的说法中,不正确的是( )
一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示.下列关于该反应的说法中,不正确的是( )
 一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示.下列关于该反应的说法中,不正确的是( )
一定条件下,在一个密闭容器内发生某反应,测得反应前后各物质的质量如图所示.下列关于该反应的说法中,不正确的是( )| A. | Q物质是由碳、氢、氧三种元素组成 | |
| B. | 该反应既不是化合反应,也不是分解反应 | |
| C. | X的值是44 | |
| D. | 生成的水的质量为36 g |
11.下列物质中,不属于合金的是( )
| A. | 不锈钢 | B. | 纯铁 | C. | 硬铝 | D. | 生铁 |
