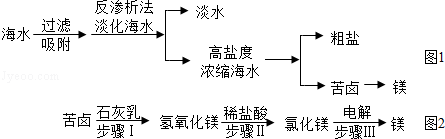
题目内容
13.学习化学过程中需要经常做实验.下列实验操作正确的是( )| A. |  倾倒液体 | B. |  过滤 | C. |  闻气味 | D. |  稀释浓硫酸 |
分析 根据向试管内倾倒液体的注意事项考虑;B、根据过滤时的一贴二低三靠考虑;C、根据闻气体气味的方法考虑;D、根据浓硫酸的稀释方法考虑.
解答 解:A、倾倒液体时:瓶塞倒放,试管倾斜,试管口与试剂瓶口紧挨着,标签向着手心,故A正确;
B、过滤时要用玻璃棒引流,漏斗尖嘴部分紧贴漏斗内壁,故B错;
C、闻气体气味的方法:用手扇着闻,故C错;
D、稀释浓硫酸的方法:将浓硫酸沿着容器壁慢慢倒入水中,故D错.
故选A.
点评 化学实验的基本操作是做好化学实验的基础,学生要在平时的练习中多操作,掌握操作要领,使操作规范

练习册系列答案
相关题目
3.下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是( )
| A. | O | B. | Mg | C. | N2 | D. | CO2 |
8.某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”.
实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100mL 10%的盐酸(密度为1.05g/mL)
实验步骤
(1)计算:需要37%的浓盐酸的体积为24.05mL(精确到0.01mL,下同);需要蒸馏水的体积为76.62mL(水的密度为1.0g/mL)
(2)量取浓盐酸和蒸馏水.
(3)混合配制.
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
(1)表中△t1的值为0.
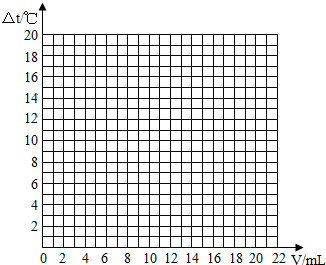
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图.
(3)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是随着中和反应的进行,由于反应放热,溶液温度上升.
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素).
横坐标及猜想理由:5,当恰好完全反应时,放出热量的最大值与原实验相同,此时所需20%的盐酸的体积是原来的二分之一;
纵坐标及猜想理由:大于18.2的值,当恰好完全反应时,放出热量的最大值与原实验相同,此时实验总质量比原实验小,所以△t最大值大于18.2℃.

实验用品:37%的浓盐酸(密度为1.18g/mL)、10%的氢氧化钠溶液、蒸馏水、量筒、温度计
实验一:配制100mL 10%的盐酸(密度为1.05g/mL)
实验步骤
(1)计算:需要37%的浓盐酸的体积为24.05mL(精确到0.01mL,下同);需要蒸馏水的体积为76.62mL(水的密度为1.0g/mL)
(2)量取浓盐酸和蒸馏水.
(3)混合配制.
实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
| 加入盐酸的体积(V)/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 | 18 | 20 |
| 溶液温度变化(△t)/℃ | △t1 | 5.2 | 9.6 | 12.0 | 16.0 | 18.2 | 16.7 | 15.7 | 14.7 | 13.7 | 12.9 |
(2)试绘出溶液温度变化与加入盐酸体积之间的关系图.
(3)根据所绘曲线分析,加入盐酸的体积在0~10mL时,溶液温度变化的趋势及其原因是随着中和反应的进行,由于反应放热,溶液温度上升.
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线最高点的位置(不考虑溶液密度和比热容的变化及热量散失等影响因素).
横坐标及猜想理由:5,当恰好完全反应时,放出热量的最大值与原实验相同,此时所需20%的盐酸的体积是原来的二分之一;
纵坐标及猜想理由:大于18.2的值,当恰好完全反应时,放出热量的最大值与原实验相同,此时实验总质量比原实验小,所以△t最大值大于18.2℃.
2.下列叙述中,属于物质的化学性质的是( )
| A. | 水在通常情况下是无色、无味的液体 | |
| B. | 铜在潮湿的空气中表面会生铜绿 | |
| C. | 将甘蔗榨成甘蔗汁 | |
| D. | 将记录有机密信息的纸张粉碎 |
1.自然界中的“氧循环”,下列说法正确的是( )
| A. | 自然界中产生氧气的途径主要是植物的光合作用 | |
| B. | “氧循环”指得是氧气的循环,多是物理变化 | |
| C. | 对于相对稳定的大气来说“氧循环”有没有无所谓 | |
| D. | 物质在空气中的缓慢氧化是释放氧气的过程 |