题目内容
通过实验制取并验证二氧化碳的某些性质.

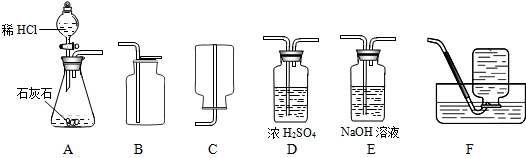
①开始实验前装置如图所示,M处应盛放______.打开活塞K,观察到的现象是______,发生反应的化学方程式是______.
②为了使实验结论科学、可靠,B装置的作用是______,该实验可知二氧化碳的化学性质是______.
③实验结束后,关闭活塞K,固液未分离,可能的原因是______.

①开始实验前装置如图所示,M处应盛放______.打开活塞K,观察到的现象是______,发生反应的化学方程式是______.
②为了使实验结论科学、可靠,B装置的作用是______,该实验可知二氧化碳的化学性质是______.
③实验结束后,关闭活塞K,固液未分离,可能的原因是______.
①M处应盛放块状的大理石或石灰石;
打开活塞K,观察到的现象是:大理石或石灰石表面产生大量气泡,C中的石蕊试纸不变色,D中的石蕊试纸变红色.
故填:块状的大理石或石灰石;大理石或石灰石表面产生大量气泡,C中的石蕊试纸不变色,D中的石蕊试纸变红色;CaCO3+2HCl═CaCl2+H2O+CO2↑.
②为了使实验结论科学、可靠,B装置的作用是吸收二氧化碳中的水蒸气;通过该实验可知,二氧化碳能和水反应生成碳酸,属于二氧化碳的化学性质.
故填:吸收二氧化碳中的水蒸气;二氧化碳能和水反应.
③实验结束后,关闭活塞K,如果反应物不足,没有二氧化碳气体再生成时,会导致固液不能分离.
故填:反应物不足,没有气体再生成.
打开活塞K,观察到的现象是:大理石或石灰石表面产生大量气泡,C中的石蕊试纸不变色,D中的石蕊试纸变红色.
故填:块状的大理石或石灰石;大理石或石灰石表面产生大量气泡,C中的石蕊试纸不变色,D中的石蕊试纸变红色;CaCO3+2HCl═CaCl2+H2O+CO2↑.
②为了使实验结论科学、可靠,B装置的作用是吸收二氧化碳中的水蒸气;通过该实验可知,二氧化碳能和水反应生成碳酸,属于二氧化碳的化学性质.
故填:吸收二氧化碳中的水蒸气;二氧化碳能和水反应.
③实验结束后,关闭活塞K,如果反应物不足,没有二氧化碳气体再生成时,会导致固液不能分离.
故填:反应物不足,没有气体再生成.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目