题目内容
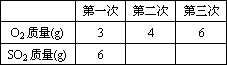
把4 g硫粉放在给定质量的氧气中燃烧,有关实验数据如下表所示.请回答下列问题:

(1)第一次实验中,参加反应的S的质量、O2的质量与生成的SO2的质量比是________.
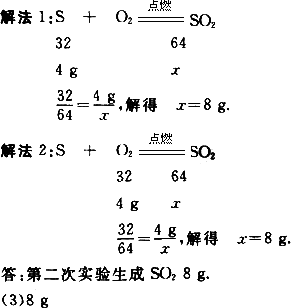
(2)请你通过计算求出第二次实验中生成SO2多少克?
(3)在表中填写第三次实验中生成SO2的质量.
答案:
解析:
解析:
|
答案:(1)1∶1∶2(或32∶32∶64或3∶3∶6) (2)因为参加反应的硫与氧气的质量比是1∶1,所以当4 g硫与4 g氧气反应时,两种物质恰好完全反应.设4 g硫粉完全反应生成二氧化硫的质量为x,则 分析:在根据化学方程式的计算中,当两种反应物的质量均为已知,求生成物的质量时,应判断所给物质硫和氧气是否都恰好完全反应.应根据化学方程式中各物质的质量比和题中所给物质的质量比来判断哪一种物质过量,然后根据完全反应的物质的质量来计算生成物的质量.由反应S+O2 |

练习册系列答案
 课时训练江苏人民出版社系列答案
课时训练江苏人民出版社系列答案 黄冈经典趣味课堂系列答案
黄冈经典趣味课堂系列答案 启东小题作业本系列答案
启东小题作业本系列答案
相关题目