题目内容
3.超市卖的纯碱产品中往往会含有少量的氯化钠,化学兴趣小组的同学要通过实验来测定某品牌的纯碱样品中纯碱的质量分数.他们实验的过程和数据如图所示,请计算: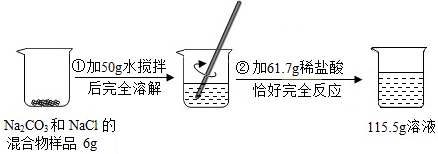
(1)生成二氧化碳多少克?
(2)样品中纯碱的质量分数是多少?
(3)反应后烧杯中氯化钠溶液的质量分数是多少?(计算结果精确至0.1%)
分析 (1)根据质量守恒定律计算反应后生成的二氧化碳的质量;
(2)根据二氧化碳的质量结合化学方程式计算碳酸钠的质量,再计算质量分数;
(3)根据质量守恒定律计算出反应后溶液的质量,溶质的质量,然后计算溶质质量分数.
解答 解:(1)根据质量守恒定律可知,生成的为:6g+50g+61.7g-115.5g=2.2g;
(2)解:设6g纯碱样品中含碳酸钠的质量为x,反应后生成的氯化钠质量为y,
Na2CO3+2HCl═2NaCl+CO2↑+H2O
106 117 44
x y 2.2g
$\frac{106}{x}$=$\frac{117}{y}$=$\frac{44}{2.2g}$
x=5.3g,y=5.85g
所以该样品中纯碱的质量分数=$\frac{5.3g}{6g}$×100%=88.3%;
反应后氯化钠的质量为:5.85g+(6g-5.3g)=6.55g,
溶液的质量为115.5g,
所以反应后烧杯中氯化钠溶液的质量分数为:$\frac{6.55g}{115.5g}$×l00%=5.7%
答:产生二氧化碳为2.2g,样品中含纯碱的质量分数为88.3%,反应后烧杯中氯化钠溶液的质量分数为5.7%.
点评 本题主要考查根据化学方程式的计算,难度不大,需要首先搞清反应原理,然后结合题中所给的数据进行解答.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案
相关题目
13.下列气体中,即能用浓硫酸干燥,又能用固体氢氧化钠干燥的是( )
| A. | CO2 | B. | SO2 | C. | H2 | D. | NH3 |
14.下列有关概念的辨析中正确的是( )
| A. | 一种元素只能组成一种单质 | |
| B. | 原子不能保持物质的化学性质 | |
| C. | 带有电荷的微粒可能不是离子 | |
| D. | 元素的种类是由原子的最外层电子数决定的 |
18. 如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
 如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )
如图是某同学对身边的一些物质测出的pH示意图,有关说法正确的是( )| A. | 葡萄汁能使紫色石蕊试液变蓝 | B. | 施用草木灰可以降低土壤碱性 | ||
| C. | 鸡蛋清的碱性比牙膏强 | D. | 胃酸过多的人不宜多食泡菜 |
8.菜地里绿色蔬菜叶片边缘发黄,小民根据所学化学知识建议父母买化肥改善现状,以获得好收成.他提出买的化肥是( )
| A. | Na2SO4 | B. | CO(NH2)2 | C. | KCl | D. | Ca3(PO4)2 |
15.下列变化属于物理变化的是( )
| A. | 氨水挥发 | B. | 铁锅生锈 | C. | 碳铵分解 | D. | 油米霉变 |
12.下列实验现象描述错误的是( )
| A. | 铁丝在氧气中燃烧火星四射 | |
| B. | 硫在氧气中燃烧产生蓝紫色火焰 | |
| C. | 红磷在氧气中燃烧产生白雾 | |
| D. | 铁丝浸入硫酸铜溶液表面有红色物质生成 |