题目内容
某校化学兴趣小组同学用一瓶含有少量氯化钠的硫酸钠固体样品,进行如下图所示的实验。
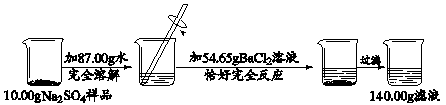
已知:Na2SO4 + BaCl2 == BaSO4↓ + 2NaCl
请根据以上信息,计算反应后所得溶液中溶质的质量分数。
解:生成BaSO4的质量为:10g + 87g + 54.65g - 140g = 11.65 g
设样品中硫酸钠的质量为x,生成氯化钠的质量为y
Na2SO4 + BaCl2  BaSO4↓ + 2NaCl
BaSO4↓ + 2NaCl
142 233 117
x 11.65g y
 x = 7.1g
x = 7.1g
 y = 5.85
y = 5.85 g
g
反应后溶液中溶质的质量为:(10g-7.1g)+ 5.85g = 8.75g
= 8.75g
反应后溶液中溶质的质量分数为:
答:反应后所得溶液中溶质的质量分数为6.25%。

练习册系列答案
相关题目
 (2012?荔湾区一模)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示.
(2012?荔湾区一模)某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到10g水垢中,产生CO2气体的情况如图所示.  某校化学兴趣小组同学在实验测定一块大理石中碳酸钙的质量分数.他们称取的大理石质量为12.5g,将其放入足量的稀盐酸中,产生气体的情况如图所示.计算该大理石中碳酸钙的质量分数?(大理石中除碳酸钙之外的其它杂质不与盐酸发生反应)
某校化学兴趣小组同学在实验测定一块大理石中碳酸钙的质量分数.他们称取的大理石质量为12.5g,将其放入足量的稀盐酸中,产生气体的情况如图所示.计算该大理石中碳酸钙的质量分数?(大理石中除碳酸钙之外的其它杂质不与盐酸发生反应) 某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢后,产生CO2气体的情况如图所示.
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁.他们为了测定水垢中碳酸钙的含量,将足量质量分数为10%的盐酸加入到12.5g水垢后,产生CO2气体的情况如图所示.