题目内容
11. 根据图的信息判断,下列说法错误的是( )
根据图的信息判断,下列说法错误的是( )| A. | 硫元素属于非金属元素 | B. | 硫原子的核电荷数为16 | ||
| C. | 硫原子的相对原子质量为32.07 | D. | 硫离子的最外层电子数为6 |
分析 根据原子结构示意图的特点:稀有气体元素,原子最外层电子数为8(氦为2 ),为稳定结构;金属元素的最外层电子数一般少于4;易失去电子成为阳离子;非金属元素的最外层电子数一般多于4,易得到电子,形成阴离子;进行分析解答本题
解答 解:
A、根据原子结构示意图的特点:非金属元素的最外层电子数一般大于4;可推断该元素属于非金属元素;故正确;
B、根据原子的结构示意图可知硫原子核内有16个质子,核电荷数为16,故正确;
C、根据元素周期表可知硫原子的相对原子质量为32.07,故正确;
D、根据原子的结构示意图可知硫原子的最外层电子数是6,故错误.
故选D.
点评 本题考查学生对原子结构示意图的特点的理解与掌握,并能在解题中灵活应用.

练习册系列答案
相关题目
1.下列溶液的pH值最大的是( )
| A. | 石灰水 | B. | 食醋 | C. | 食盐水 | D. | 汽水 |
2.化学与社会生活密切相关,下列说法错误的是( )
| A. | 不能用铁制容器配制波尔多液(含有氢氧化钙和硫酸铜) | |
| B. | 煤炉上放一壶水可以防止煤气中毒 | |
| C. | 缺锌者可以在医生指导下通过口服葡萄糖酸锌溶液来补充,锌属于人体必需的微量元素 | |
| D. | 生铁和钢都是铁的合金,是目前使用最多的金属材料,都属于混合物 |
19.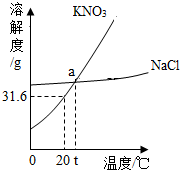 如图是KNO3和NaCl的溶解度曲线,以下说法不正确的是( )
如图是KNO3和NaCl的溶解度曲线,以下说法不正确的是( )
 如图是KNO3和NaCl的溶解度曲线,以下说法不正确的是( )
如图是KNO3和NaCl的溶解度曲线,以下说法不正确的是( )| A. | a点表示的含义:t℃,KNO3和NaCl的溶解度相等 | |
| B. | KNO3饱和溶液中含有少量的NaCl,可采用降温结晶法提纯KNO3 | |
| C. | 20℃,向50 g水中加入16 g KNO3,可得到66 g KNO3溶液 | |
| D. | 将t℃时两种物质的饱和溶液降温到20℃,所得溶液的质量分数NaCl大于KNO3 |
16.下列物质能在pH=1的溶液中共存且形成无色溶液的是( )
| A. | (NH4)2SO4、NaNO3、KCl | B. | K2SO4、KNO3、KMnO4 | ||
| C. | Na2SO4、NaCl、Na2CO3 | D. | BaCl2、NaNO3、K2SO4 |
3.向AgNO3和Cu(NO3)2混合溶液中加入一定量的锌粉,充分反应后再加入稀盐酸无明显现象.下列说法正确的是( )
| A. | 一定有锌粉剩余 | B. | 所得溶液中一定有Zn2+ | ||
| C. | 一定有银粉生成 | D. | 所得溶液中一定有Cu2+、Ag+ |
20.已知碳化硅中碳元素显-4价,硅元素显+4价,则碳化硅的化学式为( )
| A. | SiC | B. | Si2C3 | C. | Si3C2 | D. | SiC2 |
1.工业上用氨气(NH3)制取硝酸(HNO3),工业流程中核心化学反应依次为:
①4NH3+5O2$\frac{\underline{\;\;△\;\;}}{\;}$4NO+6H2O
②2NO+O2=2NO2
③3NO2+H2O=2HNO3+NO
下列判断不正确的是( )
①4NH3+5O2$\frac{\underline{\;\;△\;\;}}{\;}$4NO+6H2O
②2NO+O2=2NO2
③3NO2+H2O=2HNO3+NO
下列判断不正确的是( )
| A. | ①的生成物均为氧化物 | |
| B. | 三个反应均不属于基本反应类型 | |
| C. | 通常情况下一氧化氮不与水反应 | |
| D. | 制取硝酸过程中产生的NO应循环使用 |
 A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):
A、B、C、D都是初中化学中常见物质,A是人类赖以生存的一种无色液体,D是一种黑色固体,具有如图所示的转化关系(反应条件、其他反应物及多余产物均略去):