题目内容
12. 已知 Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl 组成的固体混合物.向其中逐渐滴加溶质质分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:
已知 Na2CO3的水溶液呈碱性,在一烧杯中盛有20.4g Na2CO3和NaCl 组成的固体混合物.向其中逐渐滴加溶质质分数为10%的稀盐酸.放出气体的总质量与所滴入稀盐酸的质量关系曲线如下图所示,请根据题意回答问题:(1)当滴加稀盐酸至图中B点时溶液中的溶质是:NaCl和HCl(填化学式),烧杯中溶液的pH<7(填>、=、<).
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),通过计算求出其中溶质的质量分数.(计算结果的保留到0.1%位)
分析 (1)加入盐酸至A点是气体不再产生,也就是恰好完全反应,继续滴加盐酸,盐酸过量,所以B点时溶质为氯化钠和氯化氢,溶液显酸性,pH小于7;
(2)根据消耗的盐酸的质量和对应的化学方程式求算反应的碳酸钠的质量和生成的氯化钠的质量,进而求算所得溶液中氯化钠的质量分数.
解答 解:(1)加入盐酸至A点是气体不再产生,也就是恰好完全反应,继续滴加盐酸,盐酸过量,所以B点时溶质为氯化钠和氯化氢,溶液显酸性,pH小于7;
(2)设A点时消耗的HCl的质量10%×73g=7.3g
设参加反应的碳酸钠的质量为x,生成的氯化钠的质量为y,生成的二氧化碳的质量为z
Na2CO3+2HCl═2NaCl+H2O+CO2↑
106 73 117 44
x 7.3g y z
$\frac{106}{x}$=$\frac{73}{7.3g}$=$\frac{117}{y}$=$\frac{44}{4.4g}$
x=10.6g
y=11.7g
z=4.4g
所得溶液中氯化钠的质量分数为$\frac{20.4g-10.6g+11.7g}{20.4g+73g-4.4g}$×100%≈24.2%
答:(1)当滴加稀盐酸至图中B点时溶液中的溶质是:NaCl和HCl,烧杯中溶液的pH<7;
(2)当滴加稀盐酸至图中A点时,烧杯中为不饱和溶液(常温),其中氯化钠的质量分数为24.2%.
点评 根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程要完整.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
2.将等质量的氢氧化钠溶液(质量分数为a%)与盐酸溶液(质量分数为b%)混合充分反应后,滴入石蕊试液后不变色,则a与b的关系是( )
| A. | a>b | B. | a<b | C. | a=b | D. | 无法确定 |
20.用过滤方法提纯粗盐时,滤纸上留下的物质是( )
| A. | 食盐 | B. | 食盐与不溶性杂质 | ||
| C. | 不溶性杂质 | D. | 无任何物质 |
7.有关科研机构预测今年的冬季将比往年冷.我国北方某些城市曾用食盐融雪,造成土壤中含盐浓度偏高,使路旁树木死亡.目前专家已研制出一种新型融雪剂,既能融化冰雪,又能起施肥美化树木的作用.具有上述作用的新型融雪剂是( )
| A. | 氯化钠、氯化钙 | B. | 氯化钠、氯化镁 | ||
| C. | 氯化钠、碳酸镁 | D. | 尿素、硝酸钙、硝酸镁 |
17.下列对某一主题知识归纳全部正确的是( )
| A. | 性质与用途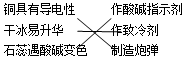 | B. | 生活常识 | ||
| C. | 科学之最 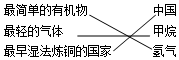 | D. | 科学中的“三”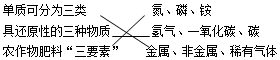 |
1.为了除去碳酸钙固体(难溶于水)中的碳酸钠杂质(能溶于水),下面操作方法正确的是( )
| A. | 直接过滤 | B. | 溶解后过滤 | C. | 溶解后蒸馏 | D. | 直接蒸馏 |
2.有X、Y、Z三种金属,将Z和Y浸入稀硫酸中,Y溶解,Z不溶解;将Z浸入X的硝酸盐溶液中,其表面有X析出,这三种金属的活动顺序是( )
| A. | X>Z>Y | B. | X>Y>Z | C. | Y>Z>X | D. | Y>X>Z |