��Ŀ����
����Ŀ���������Ϲ㷺Ӧ�������������С�
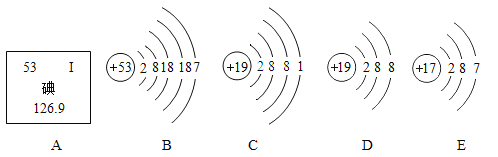
(1)�����¼����ܽ�����ּӹ��������Ľ���˿,����������άһ���֯�������������ͱ�������,���������˲���ֵ�_________________________(����ĸ)��
A.������
B.��չ��
C.��ʴ��
(2)��������Ʒ������Ҫ������_________________________�����˻�ѧ��Ӧ��
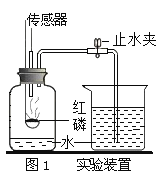
(3)��̽������ͭ�����Ľ������˳��ʱ,ijС���������ͼ������ʵ��(���ý�������״���С��ͬ):
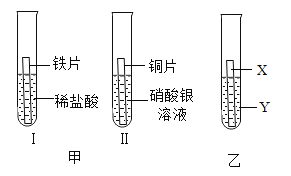
��ʵ��II�з�����Ӧ��������_________________________��
��������ͼ������ʵ�鲻�ܵó����ֽ����Ļ��˳��,��Ҫ����һ������ͼ��ʾʵ��(���ü�ͼ�е�ijЩҩƷ),��X�ǽ���_________________________��Y��_________________________��
(4)ij��ѧ��ȤС��Ϊ�ⶨij��ͭ(�������ͭ��п)��ͭ�ĺ���������ʵ��:��ȡ20g��ͭ��ĩ���ձ���,��60gϡ����ƽ�������μ��룬��ַ�Ӧ����ʵ�����ݼ��±�:
��һ�� | �ڶ��� | ������ | |
��Ӧ���ձ���ʣ�����ʵ��� | 39.92 | 59.84 | 79.80 |
��60gϡ����ȫ������,��Ӧ�����ɵ�������������_________________________g��
���û�ͭ��Ʒ��ͭ������������_________________________��
���𰸡�B ������ˮ����(��O2 ��H2O) ͭƬ����������ɫ������������Һ����ɫ��Ϊ��ɫ ͭƬ ϡ���� 0.2 67.5%
��������
(1)����ּӹ��������Ľ���˿����Ҫ�������˲���ֵ���չ�ԡ�
(2) ����Ʒ��ʴ�Ĺ���,ʵ��������������е�������ˮ�����ȷ�����ѧ��Ӧ�Ĺ��̡�
(3)��ͭ����������Һ��Ӧ������������ͭ,��˿ɹ۲쵽������ΪͭƬ����������ɫ��������,��Һ����ɫ��Ϊ��ɫ;
����ͼ�еõ�����Ϣ���ڽ������˳�������������ǰ��,ͭ��������ǰ��,������ͭ��������λ�ù�ϵ�����,����ȡ��Ƭ������������Һ��,��������ͭ��λ�ù�ϵ�Բ��ܵó��������ͭƬ����ϡ������,����ͭ�������ߵĻ��˳����ܵó����������ɣ���
(4)��ͭ��п�м���ϡ���ᣬͭ��������Ӧ,п��ϡ���ᷴӦ��������п����������һ�η�Ӧ��������������Ϊ![]() ,���ڶ��η�Ӧ�����ɵ���������Ϊ
,���ڶ��η�Ӧ�����ɵ���������Ϊ![]() ,�������η�Ӧ�����ɵ���������Ϊ
,�������η�Ӧ�����ɵ���������Ϊ![]() ���ڱȽϵ�-�κ͵ڶ��η�Ӧ��������������,��ϡ������ȫ��Ӧʱ,���Եó�ÿ����20 gϡ����,��������������ӦΪ0.08 g,�������μ���20 gϡ����ʱ,���ɵ���������0.08 g,˵����ʱϡ���Ტû����ȫ��Ӧ�������е�п����ȫ��Ӧ����������0.2 g��
���ڱȽϵ�-�κ͵ڶ��η�Ӧ��������������,��ϡ������ȫ��Ӧʱ,���Եó�ÿ����20 gϡ����,��������������ӦΪ0.08 g,�������μ���20 gϡ����ʱ,���ɵ���������0.08 g,˵����ʱϡ���Ტû����ȫ��Ӧ�������е�п����ȫ��Ӧ����������0.2 g��
�⣺��μӷ�Ӧп������Ϊx��
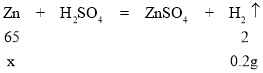
![]() x=6.5g
x=6.5g
�μӷ�Ӧ��п������Ϊ6.5g��
�û�ͭ��.Ʒ��ͭ����������Ϊ![]()
![]() ��
��

 ����������������ϵ�д�
����������������ϵ�д�����Ŀ��ijѧУ��ѧϰС��Ե��ص�ʯ��ʯ�������е��飬�ⶨʯ��ʯ��̼��Ƶ��������������õķ������£�ȡ��ʯ��ʯ��Ʒ16g����80gϡ������Ĵμ��룬���������������ݼ��±�����֪ʯ��ʯ��Ʒ�к��еĶ�����������ʲ�����ˮ������ϡ���ᷴӦ��������㣺
��� | ����ϡ���������/g | ʣ����������/g |
��1�� | 20 | 11 |
��2�� | 20 | 6 |
��3�� | 20 | 2.8 |
��4�� | 20 | n |
��1���ϱ���n����ֵΪ ��
��2����Ʒ��̼��Ƶ����������� ��
��3�������������ʵ�����������