题目内容
(1)实验室用电解水的实验来探究水的组成.请写出检验正极产生的气体的操作、现象和结论______.
(2)实验室电解水时通常向水中加入少量的稀硫酸,以增强导电性.若电解前加入的稀硫酸与水混合后,硫酸的质量分数为8%.取180g这样的溶液进行电解,当溶液中硫酸的质量分数为10%时,参加电解的水的质量______g.
(3)若电解消耗18g的水,则可得氧气多少体积?(假设该状态下氧气的密度为1.4g/L)请写出完整的计算过程.(除不尽保留1位小数)
解:(1)由于电解水时正极会生成氧气,而氧气能使带火星的木条复燃,所以检验正极产生的气体的操作、现象和结论是用带火星的木条伸入,木条复燃剧烈燃烧,则该气体是氧气;
(2)设被电解的水的质量为x.
180g×8%=(180g-x)×10%
解得x=36g;
(3)设可得到O2的质量为x
2H2O 2H2↑+O2↑
2H2↑+O2↑
36 32
18g x
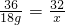
x=16g
得到的氢气标况下的体积V氧气= =11.4 L;
=11.4 L;
故答案为:(1)用带火星的木条伸入,木条复燃剧烈燃烧,则该气体是氧气;(2)36;(3)若电解消耗18g的水,则可得氧气的体积为11.4L;
分析:(1)依据电解水时正极产生的气体是氧气分析解答;
(2)本题实际上是溶液浓缩问题.8%的硫酸溶液中溶质质量跟10%的硫酸溶液中溶质质量相等,由此可计算出被电解的水的质量.
(3)依据化学方程式的相关基本计算和气体的质量与体积的转化关系分析判断;
点评:此题是对电解水有关问题的考查,解题的关键是掌握水的电解实验的有关结论以及根据反应的化学方程式的基本计算.
(2)设被电解的水的质量为x.
180g×8%=(180g-x)×10%
解得x=36g;
(3)设可得到O2的质量为x
2H2O
 2H2↑+O2↑
2H2↑+O2↑36 32
18g x
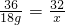
x=16g
得到的氢气标况下的体积V氧气=
 =11.4 L;
=11.4 L;故答案为:(1)用带火星的木条伸入,木条复燃剧烈燃烧,则该气体是氧气;(2)36;(3)若电解消耗18g的水,则可得氧气的体积为11.4L;
分析:(1)依据电解水时正极产生的气体是氧气分析解答;
(2)本题实际上是溶液浓缩问题.8%的硫酸溶液中溶质质量跟10%的硫酸溶液中溶质质量相等,由此可计算出被电解的水的质量.
(3)依据化学方程式的相关基本计算和气体的质量与体积的转化关系分析判断;
点评:此题是对电解水有关问题的考查,解题的关键是掌握水的电解实验的有关结论以及根据反应的化学方程式的基本计算.

练习册系列答案
相关题目

