题目内容
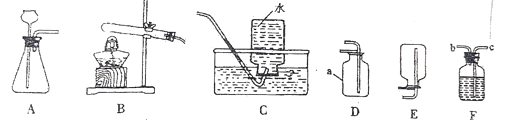
【题目】同学们在学校一定做过这些实验,现提供下列装置:
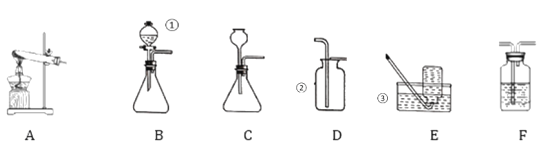
Ⅰ.实验室制备氧气
(1)请写出实验仪器的名称:①是________;②是_______;③是________。
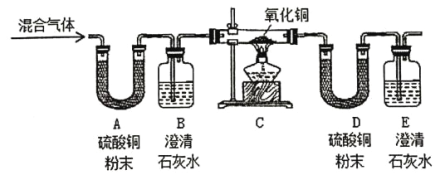
(2)实验室用高锰酸钾制取氧气,发生装置A应做的改动是______,反应的化学方程式为______________________,若用E装置收集氧气,当有______时,开始收集气体。
Ⅱ.实验室制二氧化碳
(1)按照“C→F→F→真空气囊”的装置顺序制取纯净的CO2气体,C装置中发生反应的化学方程式为_____________,第一个F装置盛放试剂为______第二个F装置盛放的作用是__________________________________。
(2)若将C换成B装置,B的优点是_______________________。
Ⅲ.配制稀盐酸
(1)用市售浓盐酸(溶质质量分数为37%,密度为1.2g/ml)配制500g溶质质量分数为12%的稀盐酸,需要浓盐酸___ml(保留一位小数),量取水时应选用的量筒是____(选填字母)
A 100ml量筒 B 250ml量筒 C 500ml量筒
(2)下列操作中,可能导致配制稀盐酸的溶质质量分数偏大的是______(填字母)。
A 将浓盐酸导入量筒时,洒出少许
B 量取水时俯视读数
C 用不干燥的烧杯稀释盐酸
D 将配好的溶液转移到吸口瓶时,有少量溶液溅出
【答案】分液漏斗 集气瓶 水槽 试管口放一团棉花 2KMnO4![]() K2MnO4+MnO2+O2↑ 气泡均匀连续冒出
K2MnO4+MnO2+O2↑ 气泡均匀连续冒出 ![]() 饱和碳酸氢钠溶液 浓硫酸 可以控制反应的速率 135.1 C b
饱和碳酸氢钠溶液 浓硫酸 可以控制反应的速率 135.1 C b
【解析】
Ⅰ.实验室制备氧气
(1)分液漏斗可以控制反应的速率,集气瓶是收集气体的仪器,水槽是盛水的仪器,故答案为:分液漏斗;集气瓶;水槽;
(2)加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;故答案为:试管口放一团棉花;2KMnO4![]() K2MnO4+MnO2+O2↑;气泡均匀连续冒出;
K2MnO4+MnO2+O2↑;气泡均匀连续冒出;
Ⅱ.实验室制二氧化碳
(1)碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;饱和碳酸氢钠溶液可以除去氯化氢气体;浓硫酸除去水蒸气,要先除杂质后干燥;故答案为:![]() ;饱和碳酸氢钠溶液;浓硫酸;
;饱和碳酸氢钠溶液;浓硫酸;
(2)若将C换成B装置,B的优点是:可以控制反应的速率;故答案为:可以控制反应的速率;
Ⅲ.配制稀盐酸
(1)设需要浓盐酸为x,1.2g/mLx×37%=500g×12%,x≈135.1mL;需要水的质量=500g-1.2g/mL×135.1mL≈337.9g,水的密度是1g/mL,约为337.9mL,因此需要用500mL的量筒;故答案为:135.1;C;
(2)A将浓盐酸导入量筒时,洒出少许,会导致质量分数偏小;
B量取水时俯视读数,水量少了,会导致质量分数偏大;
C用不干燥的烧杯稀释盐酸,水的质量增大,会导致质量分数偏小
D将配好的溶液转移到吸口瓶时,有少量溶液溅出,不会影响质量分数的变化。
故选B。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】已知:20℃时,NaCl和NaNO3的溶解度分别为36 g和88 g。
| 序号 | ① | ② | ③ | ④ | ⑤ |
固体种类 | NaCl | NaCl | NaNO3 | NaNO3 | NaNO3 | |
固体的质量/g | 30 | 60 | 30 | 60 | 90 | |
水的质量/g | 100 | 100 | 100 | 100 | 100 |
上表是20℃时实验得出的数据,根据该数据,则下列关于①~⑤所得溶液的说法不正确的是
A. 溶质质量:②=④B. 溶液质量: ①<②
C. 溶质质量分数:①=③D. ⑤中溶质与溶剂的质量比为22:25