题目内容
 小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定.他们从瓶中取出该溶液共51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示:
小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定.他们从瓶中取出该溶液共51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示:(1)生成氧气的质量;
(2)则该溶液中所含双氧水的质量分数是多少?
分析:根据题意和生成氧气的质量与反应时间的关系图,完全反应后生成氧气的质量为0.48g,据此根据反应的化学方程式计算出过氧化氢的质量,进而计算出该溶液中所含双氧水的质量分数即可.
解答:解:(1)由图象可知,完全反应后生成氧气的质量为0.48g.
(2)设参与反应的H2O2的质量为x,
2H2O2
2H2O+O2↑
68 32
x 0.48g
=
x=1.02g
×100%=2%.
答:(1)生成氧气的质量为0.48g;(2)该溶液中所含双氧水的质量分数是2%.
(2)设参与反应的H2O2的质量为x,
2H2O2
| ||
68 32
x 0.48g
| 68 |
| 32 |
| x |
| 0.48g |
| 1.02g |
| 51g |
答:(1)生成氧气的质量为0.48g;(2)该溶液中所含双氧水的质量分数是2%.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,细致地分析题意(或图示信息)等各种信息是正确解答本题的前提和关键.

练习册系列答案
相关题目
 过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定溶质质量分数.他们取出该溶液51g,加入适量二氧化锰,生成气的质量与反应时间的关系如图所示.
过氧化氢溶液长期保存会自然分解,使得溶质质量分数减小.小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定溶质质量分数.他们取出该溶液51g,加入适量二氧化锰,生成气的质量与反应时间的关系如图所示. 小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定.他们从瓶中取出该溶液共51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示:则该溶液中所含双氧水的实际质量是多少克?
小军从家中拿来一瓶久置的医用过氧化氢溶液,和同学们一起测定.他们从瓶中取出该溶液共51g,加入适量二氧化锰,生成氧气的质量与反应时间的关系如图所示:则该溶液中所含双氧水的实际质量是多少克?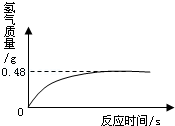 2012年“世界水日”的宣传主题是水与链式安全,水是生命之源,我们应该水,爱护水资源.某化学兴趣小组对某地水质状况进行了相关研究调查:
2012年“世界水日”的宣传主题是水与链式安全,水是生命之源,我们应该水,爱护水资源.某化学兴趣小组对某地水质状况进行了相关研究调查: