题目内容
气体的实验室制法是一种重要的实验基本技能,请回顾二氧化碳的实验室制法,回答下列问题:
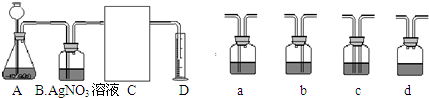
(1)下面是二氧化碳的制取、净化、收集和量气的相关实验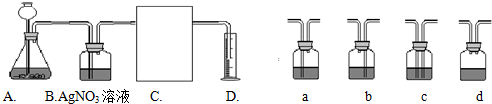
(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是 .
②实验过程B装置产生的主要实验现象是: ;涉及化学反应是 .
③方线框中的C装置应该选择上面提供的a、b、c、d的 .
(1)下面是二氧化碳的制取、净化、收集和量气的相关实验

(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是
②实验过程B装置产生的主要实验现象是:
③方线框中的C装置应该选择上面提供的a、b、c、d的
分析:①长颈漏斗的颈部没有开关,分液漏斗的颈部有开关;
②盐酸易挥发,挥发出的氯化氢气体和二氧化碳一起导出;
③根据a、b、c、d装置的组装特点,可以判断方线框中的C装置应该选择的装置.
②盐酸易挥发,挥发出的氯化氢气体和二氧化碳一起导出;
③根据a、b、c、d装置的组装特点,可以判断方线框中的C装置应该选择的装置.
解答:解:①使用分液漏斗,可以控制稀盐酸的滴加速率,从而控制反应速率,而长颈漏斗不具备这一特点.
故填:可以控制稀盐酸的滴加速率,从而控制反应速率.
②当氯化氢进入硝酸银溶液中时,能和硝酸银反应生成氯化银沉淀和硝酸,反应的化学方程式为:AgNO3+HCl═AgCl↓+HNO3.
故填:产生白色沉淀;AgNO3+HCl═AgCl↓+HNO3.
③b、c装置中,气体无法导出,d装置中,不能除去氯化氢气体;
a装置中,氯化氢气体能够被碳酸氢钠溶液吸收,二氧化碳能够导出,所以应该选择a装置.
故填:a.
故填:可以控制稀盐酸的滴加速率,从而控制反应速率.
②当氯化氢进入硝酸银溶液中时,能和硝酸银反应生成氯化银沉淀和硝酸,反应的化学方程式为:AgNO3+HCl═AgCl↓+HNO3.
故填:产生白色沉淀;AgNO3+HCl═AgCl↓+HNO3.
③b、c装置中,气体无法导出,d装置中,不能除去氯化氢气体;
a装置中,氯化氢气体能够被碳酸氢钠溶液吸收,二氧化碳能够导出,所以应该选择a装置.
故填:a.
点评:碳酸氢钠能和氯化氢反应生成氯化钠、水和二氧化碳,从而把二氧化碳中的氯化氢气体除去,生成的二氧化碳和原来的二氧化碳一起导出.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案
相关题目
气体的实验室制法是一种重要的实验基本技能,请回顾二氧化碳的实验室制法,回答下列问题:
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2 CO2
CO2
②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4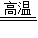 CaO+CO↑+CO2↑
CaO+CO↑+CO2↑
⑤CO+Fe2O3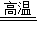 2Fe+3CO2
2Fe+3CO2
…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:______.现提供有①纯净的CaCO3白色粉末,②大理石,③稀盐酸,③浓盐酸,④稀硫酸,⑤浓硫酸.其中最适合用于实验室制取二氧化碳的药品是______(填代号)
(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
①分析上述数据可得到一个结论:______;盐酸是氯化氢气体溶于水得到的溶液,升高盐酸溶液的温度,其密度将变______.
②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸______ml.配制过程中要用到量筒、______、烧杯、玻璃棒等仪器.
(3)下面是二氧化碳的制取、净化、收集和量气的相关实验
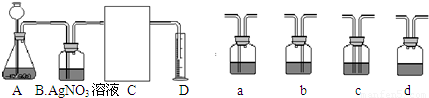
(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是______
②实验过程B装置产生的主要实验现象是:______;
涉及化学反应是______.
③方线框中的C装置应该选择上面提供的a、b、c、d的______.
(1)化学反应能生成二氧化碳的反应很多,如见下面反应
①C+O2
 CO2
CO2②Na2CO3+2HCl=2NaCl+H20+CO2↑
③CaCO3+2HCl=2CaCl2+H20+CO2↑
④CaC2O4
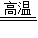 CaO+CO↑+CO2↑
CaO+CO↑+CO2↑⑤CO+Fe2O3
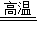 2Fe+3CO2
2Fe+3CO2…
请任意分析上面一个不适合于实验制取二氧化碳的反应的原因:______.现提供有①纯净的CaCO3白色粉末,②大理石,③稀盐酸,③浓盐酸,④稀硫酸,⑤浓硫酸.其中最适合用于实验室制取二氧化碳的药品是______(填代号)
(2)盐酸密度(20℃时)和其溶质质量分数之间的关系
| 密度(ρ)/g?ml-1 | 1.00 | 1.02 | 1.04 | 1.06 | 1.08 | 1.10 | 1.12 | 1.14 | 1.16 | 1.185 |
| 溶质质量分数(w)/% | 0.4 | 4.4 | 8.5 | 12.5 | 16.5 | 20.4 | 24.2 | 28.2 | 32.2 | 37.2 |
②现要配制200ml溶质质量分数为8.5%的稀盐酸用于制取二氧化碳,则需要溶质质量分数为37.2%的浓盐酸______ml.配制过程中要用到量筒、______、烧杯、玻璃棒等仪器.
(3)下面是二氧化碳的制取、净化、收集和量气的相关实验

(温馨提示:C装置中装饱和碳酸氢钠溶液,二氧化碳不溶于饱和碳酸氢钠溶液)
①A中的长颈漏斗如果用分液漏斗代替的好处是______
②实验过程B装置产生的主要实验现象是:______;
涉及化学反应是______.
③方线框中的C装置应该选择上面提供的a、b、c、d的______.
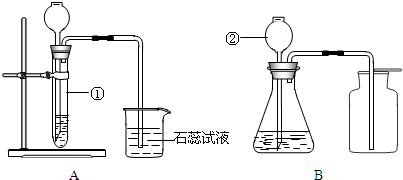 (2010?越秀区二模)某小组利用以下装置进行有关气体的实验室制法和性质的研究.
(2010?越秀区二模)某小组利用以下装置进行有关气体的实验室制法和性质的研究.