题目内容
15.造纸厂会产生含氢氧化钠的废水,需经处理呈中性后排放,为测定此废水中氢氧化钠的质量分数,小明取40g废水样品加入到锥形瓶中,逐滴加入10%的稀硫酸,至恰好完全反应时,消耗稀硫酸49g,试计算:(1)参加反应的硫酸的质量为4.9g.
(2)废水中氢氧化钠的质量分数.
分析 (1)根据溶质质量=溶液质量×溶质质量分数解答;
(2)利用恰好完全反应所消耗硫酸的质量,根据反应的化学方程式,计算废水中氢氧化钠的质量;最后利用溶液中溶质的质量分数公式计算出废水中氢氧化钠的质量分数.
解答 解:
(1)反应消耗硫酸的质量为:49 g×10%=4.9 g
设废水样品中氢氧化钠的质量为x.
2NaOH+H2SO4=Na2SO4+2H2O
80 98
x 4.9 g
$\frac{80}{x}=\frac{98}{4.9g}$
x=4g
废水中氢氧化钠的质量分数为$\frac{4g}{40g}$×100%=10%
答案:
(1)4.9g;
(2)废水中氢氧化钠的质量分数为10%
点评 本题较简单,可直接利用化学方程式来计算,但应注意计算格式要规范,向规范要质量.

练习册系列答案
相关题目
7.下列物质的用途中,利用其物理性质的是( )
| A. | 氧气用于炼钢 | B. | 硫酸用于除铁锈 | ||
| C. | 干冰用作制冷剂 | D. | 碳酸氢钠用于治疗胃酸过多症 |
10.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
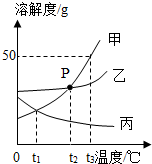

| A. | t3℃时,溶解度由大到小的顺序是甲>乙>丙 | |
| B. | 当甲中混有少量乙时,提纯甲可采用降温结晶 | |
| C. | t3℃时,将30g甲物质加入到50g水中,充分溶解后所得溶液的质量为75g | |
| D. | t2℃时等质量的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得溶液中溶剂的质量由大到小的顺序为甲=丙>乙 |
20.下列物质的用途语其性质相对应的是( )
| A. | 用稀硫酸除铁锈:稀硫酸不易挥发 | |
| B. | 干冰用于人工降雨:二氧化碳既不燃烧也不支持燃烧 | |
| C. | 用熟石灰改良酸性土壤:氢氧化钙的碱性 | |
| D. | 撒盐融雪:盐的凝固点比水高 |
7.甲和乙在一定条件下反应生成丙和丁.结合微观示意图分析,下列结论不正确的是( )
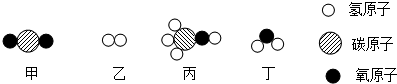

| A. | 甲、乙、丙、丁四种物质中只有乙是单质 | |
| B. | 丙是一种有机物 | |
| C. | 发生反应的甲和乙的分子个数比为1:1 | |
| D. | 一个丙分子中含有6个原子 |