题目内容
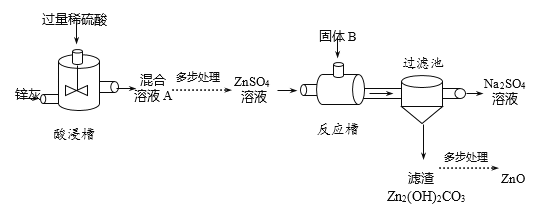
【题目】高锰酸钾是常用的氧化剂。如图是实验室模拟工业上制备高锰酸钾晶体的操作流程:

(1)完成操作③的名称是_____,所需要的玻璃仪器是______(填一种即可);
(2)操作流程中可循环利用的物质是___________。
(3)氢氧化钾、二氧化锰和氧气在高温条件下煅烧,生成锰酸钾和水,该反应的化学方程式为___________。
【答案】过滤 玻璃棒或烧杯或漏斗 二氧化锰 4KOH+2MnO2+O2![]() 2K2MnO4+2H2O
2K2MnO4+2H2O
【解析】
(1)操作③是将高锰酸钾晶体与滤液分离,是过滤操作,完成过滤操作所需要的玻璃仪器是玻璃棒、烧杯、漏斗;
(2)既是反应物,也是生成物的物质可以循环使用,由实验室模拟工业上制备高锰酸钾晶体的操作流程,则生产过程中可循环使用的物质是二氧化锰;
(3)氢氧化钾、二氧化锰和氧气在高温条件下煅烧,生成锰酸钾和水,该反应的化学方程式为4KOH+2MnO2+O2![]() 2K2MnO4+2H2O。
2K2MnO4+2H2O。

【题目】认识物质的组成和结构,进而能推知物质的性质和用途。
(1)原子结构决定元索性质。
2016年6月8日,国际纯粹与应用化学联合会正式发布113号等四种新元素的英文名称和元素符号。2017年5月9日,我国发布了这四种元素的中文名称。其中113号的元素符号为Nh,中文名称为“鉨”。如图甲、乙分别为鉨原子和铝原子结构示意图。请回答下列问题:

①在化学反应中,鉨原子形成离子的符号为________________。
②根据原子结构,理论上鉨的金属活动性比铝强,你认为可能的原因是________________。
(2)物质组成和结构决定其性质.性质决定其用途。
胃酸过多须服用抗酸药。下表为两种抗酸药的有效成分及其构成微粒:
抗胃酸药 | 复方氢氧化镁片剂 | 铝碳酸镁片 |
有效成分 | Mg( OH)2 | AlMg( OH)3CO3 |
构成微粒 | Mg2+、 OH- | Al3+、Mg2+、 OH-、 CO32- |
由于抗酸药有效成分不同,起抗酸作用(即消耗胃液中盐酸)的微粒也有差异。
①Mg( OH)2起抗酸作用的微粒是_______________(填微粒符号,下同);
②铝碳酸镁与盐酸反应的化学方程式为:![]() 。铝碳酸镁起抗酸作用的两种微粒是__________________________________。
。铝碳酸镁起抗酸作用的两种微粒是__________________________________。
【题目】某化学兴趣小组为了测定某石灰石样品中碳酸钙的质量分数,取用2.0g石灰石样品,把25.0g稀盐酸分五次加入样品中(样品中的杂质既不与盐酸反应,也不溶解于水),每次充分反应后都经过滤、干燥、称量,得实验数据如下:
实验次数 | 1 | 2 | 3 | 4 | 5 |
稀盐酸的累计加入量 | 5.0g | 10.0g | 15.0g | 20.0g | 25.0g |
剩余固体的质量 | 1.5g | m | 0.5g | 0.3g | 0.3g |
计算:
(1)m=______g。
(2)石灰石中碳酸钙的质量分数为______。
(3)2.0g石灰石样品与足量稀盐酸反应,产生二氧化碳的质量是多少?_____(写出解题过程)
【题目】学习了酸的性质后,同学们知道了硫酸可以和金属发生反应,为了探究浓硫酸是不是能和非金属反应,某兴趣小组的同学进行了如下探究。将冷的浓硫酸加入到装有碳粉的圆底烧瓶中,无明显现象,加热该混合物,有大量气泡产生,现对导出的气体成分进行验证。

[查阅资料]
①碳与浓硫酸在加热时,除了生成水之外,还生成二氧化硫和碳的一种氧化物;
②水能使无水硫酸铜变蓝;
③二氧化硫和二氧化碳都能使澄清石灰水变浑浊,其中,二氧化硫还能使紫红色的酸性高锰酸钾溶液褪色。
二氧化硫和澄清石灰水反应的化学方程式为_____。
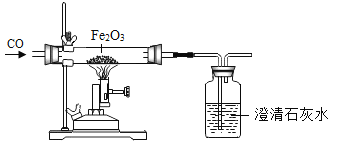
[实验验证]某化学兴趣小组在老师指导下设计了如图实验装置进行验证。
温馨提示:丁装置的A、B、C中均装有紫红色的酸性高锰酸钾溶液
①为了验证反应后的生成物,装置的正确连接顺序为:甲_____→_____→丙→_____(填序号)
②请完成表中的相关内容:
实验现象 | 实验结论 |
乙中观察到的现象_____ | 证明碳与浓硫酸加热反应生成碳的氧化物是二氧化碳而不是一氧化碳 |
丁装置A中溶液褪色,丁装置C中溶液不褪色 | 证明气体中有_____,装置C的作用_____ |
戊中白色固体变蓝 | 证明气体中有水蒸气 |
[获得结论]碳与浓硫酸加热反应的化学方程式_____。
[知识拓展]化学反应的进行与反应物的溶质质量分数、反应条件都有一定关系。酸不仅仅能与某些金属反应,还能与某些非金属单质在一定条件下反应。