题目内容
4. 如图所示,当把滴管中的甲液体滴加到小试管中乙固体上(试管底部浸没在饱和石灰水中),过一会儿可看到石灰水变浑浊了,U形管中的a液面降低,b液面升高了.根据以上现象请你分析,下列说法不正确的是( )
如图所示,当把滴管中的甲液体滴加到小试管中乙固体上(试管底部浸没在饱和石灰水中),过一会儿可看到石灰水变浑浊了,U形管中的a液面降低,b液面升高了.根据以上现象请你分析,下列说法不正确的是( )| A. | 甲、乙可能分别是稀盐酸和大理石 | |
| B. | 甲、乙可能分别是水和硝酸铵 | |
| C. | 甲、乙可能分别是水和氢氧化钠 | |
| D. | 饱和石灰水变浑浊,不一定是化学变化 |
分析 依据现象分析,石灰水变浑浊可能是生成了沉淀,也可能是温度升高导致的溶质析出,U型管的变化,说明容器内温度升高或者是生成了气体,利用这些信息可解决此题.
解答 解:
A、甲、乙分别是稀盐酸和大理石时,并与石灰水反应生成碳酸钙沉淀,U形管中的a液面降低,b液面升高,故此选项正确.
B、甲、乙有分别是水和硝酸铵时溶解吸热.温度降低,氢氧化钙溶解度升高,不会生成沉淀,会使容器内压强变小,U形管中的a液面升高,b液面降低,故此选项错误.
C、氢氧化钠固体溶于水,放出大量的热,温度升高,氢氧化钙溶解度减小,导致氢氧化钙析出,气体受热膨胀,可以出现这些现象,故正确.
D、当石灰水中析出氢氧化钙时溶液照样浑浊,发生的是物理变化,石灰水中氢氧化钙与二氧化碳反应生成碳酸钙变浑浊,发生了化学变化,故正确.
故选B.
点评 该题是一道实验综合分析题,解题的关键是对产生现象原因的分析,即:石灰水变浑浊可能是生成了沉淀,也可能是温度升高导致的溶质析出,U型管的变化,说明容器内温度升高或者是生成了气体.

练习册系列答案
 暑假作业暑假快乐练西安出版社系列答案
暑假作业暑假快乐练西安出版社系列答案
相关题目
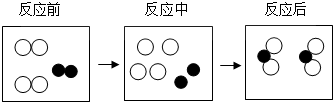
8.如图是某化学反应的微观模拟示意图( 表示一种原子,
表示一种原子, 表示另一种原子),从图中获得的有关信息不正确的是( )
表示另一种原子),从图中获得的有关信息不正确的是( )
 表示一种原子,
表示一种原子, 表示另一种原子),从图中获得的有关信息不正确的是( )
表示另一种原子),从图中获得的有关信息不正确的是( )
| A. | 化学反应中原子可以再分 | |
| B. | 化学反应中分子可以分为原子 | |
| C. | 化学反应中元素种类、原子种类和数目都没有改变 | |
| D. | 分子间存在一定的间隙 |
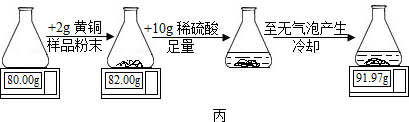
15. 石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
(1)上表中m的数值是4.4.
(2)所用盐酸溶液的溶质质量分数?
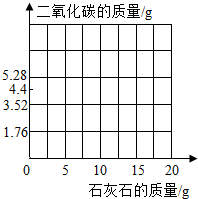
(3)在图中画出石灰石与生成二氧化碳的关系图
(4)某同学计算碳酸钙的质量分数过程如下:
设15克石灰石中碳酸钙的质量为x
根据化学方程式列关系式为:$\frac{100}{x}$=$\frac{44}{4.4g}$ 求得:x=10g,碳酸钙的质量分数为10g/15g×100%=66.7%,你认为正确么?如正确本题可不答,如不正确,请说明理由15g石灰石样品没有完全反应.
 石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:
石灰石是我省的主要矿产之一.学校研究性学习小组为了测定当地矿山石灰石中碳酸钙的质量分数,取来了一些矿石样品,并取稀盐酸200g,平均分成4份,进行实验,结果如下:| 实验 | 1 | 2 | 3 | 4 |
| 加入样品的质量/g | 5 | 10 | 15 | 20 |
| 生成CO2的质量/g | 1.76 | 3.52 | 4.4 | m |
(2)所用盐酸溶液的溶质质量分数?
(3)在图中画出石灰石与生成二氧化碳的关系图
(4)某同学计算碳酸钙的质量分数过程如下:
设15克石灰石中碳酸钙的质量为x
根据化学方程式列关系式为:$\frac{100}{x}$=$\frac{44}{4.4g}$ 求得:x=10g,碳酸钙的质量分数为10g/15g×100%=66.7%,你认为正确么?如正确本题可不答,如不正确,请说明理由15g石灰石样品没有完全反应.
12.MnO2是KClO3分解的催化剂.某化学兴趣小组发现,CuO也能加快KClO3的分解,该实验小组进行了如下探究.【提出猜想】除MnO2外,CuO也可作KClO3分解的催化剂.
【实验探究】按下表进行实验并获得相关数据
【分析数据得出结论】
(1)实验中均取用5gKClO3,目的是控制变量
(2)由实验A与实验C对比,证明猜想合理的理由是加入氧化铜后氯酸钾分解产生氧气的温度比只加热氯酸钾时产生氧气的温度低很多.
(3)相同条件下对氯酸钾分解催化效果最好的是MnO2.
【实验反思】
(1)若要确定氧化铜是该反应的催化剂,还要证明其在化学反应前后化学性质和质量不变.
(2)同种催化剂,质量多少可能影响KClO3分解的催化效果,请设计实验方案进行验证分别取相同质量的颗粒大小相同的氯酸钾,与质量不同的二氧化锰混合加热制氧气,质量多的反应的速率快.
(3)除以上因素外,还有哪些因素可能影响KClO3分解的催化效果,请再探究(探究一种因素即可)
【实验探究】按下表进行实验并获得相关数据
| 实验编号 | 实验药品及用量 | 分解温度(℃) |
| A | 5gKClO3 | 580 |
| B | 5gKClO3、1gMnO2 | 350 |
| C | 5gKClO3、1gCuO | 370 |
(1)实验中均取用5gKClO3,目的是控制变量
(2)由实验A与实验C对比,证明猜想合理的理由是加入氧化铜后氯酸钾分解产生氧气的温度比只加热氯酸钾时产生氧气的温度低很多.
(3)相同条件下对氯酸钾分解催化效果最好的是MnO2.
【实验反思】
(1)若要确定氧化铜是该反应的催化剂,还要证明其在化学反应前后化学性质和质量不变.
(2)同种催化剂,质量多少可能影响KClO3分解的催化效果,请设计实验方案进行验证分别取相同质量的颗粒大小相同的氯酸钾,与质量不同的二氧化锰混合加热制氧气,质量多的反应的速率快.
(3)除以上因素外,还有哪些因素可能影响KClO3分解的催化效果,请再探究(探究一种因素即可)
| 提出猜想 | |
| 设计方案 | |
| 得出结论 |
16.下列有关化学知识的描述正确的是( )
| A. | 催化剂不仅能改变化学反应速率,而且会增加生成物的质量 | |
| B. | 金属都能与酸溶液反应,而且反应的剧烈程度能体现金属活动性的强弱 | |
| C. | 由同种元素组成的物质一定是单质 | |
| D. | 合金的硬度一般高于它的成分金属 |
13.下列实验操作正确的是( )
| A. |  检查气密性 | B. |  测量溶液的pH | C. |  取固体药品 | D. |  稀释浓硫酸 |
14.下列试剂中,不能鉴别氯化钠溶液和稀盐酸的是( )
| A. | 石蕊试液 | B. | 酚酞试液 | C. | 金属锌 | D. | 碳酸钠溶液 |