题目内容
16.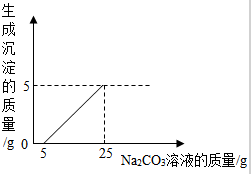 对制取二氧化碳后的溶液进行测定(假设石灰石中的杂质不与盐酸反应,也不溶于水),取一定量废液于烧杯中.向废液中慢慢滴加碳酸钠溶液,如图所示.
对制取二氧化碳后的溶液进行测定(假设石灰石中的杂质不与盐酸反应,也不溶于水),取一定量废液于烧杯中.向废液中慢慢滴加碳酸钠溶液,如图所示.(1)5g沉淀所指的物质是碳酸钙.
(2)实验所用的碳酸钠溶液中溶质的质量分数是多少?
(3)该废液中含有的溶质是CaCl2和HCl.
分析 (1)氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,故沉淀为碳酸钙;
(2)由于盐酸的量不确定,所以可以分析碳酸钠溶液质量从5g到25g的变化,由图可看出20g碳酸钠溶液和废液反应生成碳酸钙沉淀的质量为5g.可由碳酸钙的质量,根据碳酸钠与氯化钙反应的化学方程式求出碳酸钠的质量,进而求出其质量分数;
(3)石灰石和盐酸反应后所得溶液中肯定有氯化钙,若盐酸过量也可能有盐酸,可根据图中所给信息进行分析.
解答 解:(1)氯化钙与碳酸钠反应生成碳酸钙沉淀和氯化钠,故沉淀为碳酸钙;故填:碳酸钙;
(2)解:由图象可知,(25g-5g)Na2CO3溶液与氯化钙溶液全部反应,生成5g碳酸钙沉淀
设:20gNa2CO3溶液中溶质的质量为x
Na2CO3+CaCl2=CaCO3↓+2NaCl
106 100
x 5g
$\frac{106}{100}=\frac{x}{5g}$
解之得:x=5.3g
所以该Na2CO3溶液中溶质的质量分数为$\frac{5.3g}{20g}$×100%=26.5%
答:这瓶Na2CO3溶液中溶质的质量分数26.5%;
(3)所得废液是由碳酸钙和盐酸反应所得,肯定有氯化钙,由图表看出,废液和碳酸钠溶液反应开始没有沉淀生成,所以可得出废液中还有过量的盐酸.
故答案为:CaCl2、HCl
点评 解答本题的关键是要分析图表的数据对应的反应,在计算碳酸钠的质量分数时要主要数据的对应性,如所求碳酸钠的质量是通过20g碳酸钠溶液求出的,不是25g溶液

练习册系列答案
相关题目
6.下列除去杂质的方法中正确的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液、过滤 |
| B | KOH溶液 | KCl | 适量稀盐酸 |
| C | CaCl2溶液 | 稀盐酸 | 过量碳酸钙、过滤 |
| D | O2 | CO | 通过灼热的氧化铜 |
| A. | A | B. | B | C. | C | D. | D |
7.厨房中物质加入适量水后不能形成溶液的是( )
| A. | 食盐 | B. | 蔗糖 | C. | 植物油 | D. | 纯碱 |
4.新型材料的出现是材料发展史的重大突破.下列应用的材料属于复合材料的是( )
| A. |  玻璃钢茶几 | B. |  人面鱼纹彩陶盆 | C. |  金刚石薄膜 | D. |  银制器皿 |
11.下列图象与所对应操作相符的是( )
| A. | 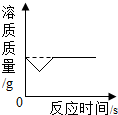 20℃时,把少量氧化钙固体放入饱和氢氧化钙溶液中 | |
| B. |  向两份相等质量、相等溶质质量分数的稀硫酸中,分别加入过量的金属Mg和Al | |
| C. | 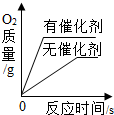 用相等质量、相等溶质质量分数的双氧水分别制取O2 | |
| D. |  向稀盐酸和氯化铜的混合溶液中加入过量的NaOH溶液 |
1.某活动小组用未知金属X和Y分别进行了两个实验,实验结果如下:(实验中所有金属局面已打磨,且形状、大小以及稀盐酸的溶质质量分数均相同)
(1)Fe、X、Y三种金属的活动性由强到弱的顺序是Fe>Y>X;
(2)取两支试管分别放入铁和金属Y,同时加入等量的稀盐酸,预期可以观察到的现象是铁和Y的表面有气泡生成,铁的表面产生的气泡快;将金属Y加入到X的硝酸盐溶液中,预期可以观察到的现象是在Y的表面有红色物质生成;
(3)现有X、Y两种金属粉末的混合物,设计实验将X和Y充分分离,写出实验操作步骤.(提示:分离混合物需加入稍过量的试剂以达到最大限度的分离)
| 实验操作 | 金属X | 金属Y |
| 分别将金属放入稀盐酸中 | 没有变化 | 有气泡生成 |
| 分别将铁片插入金属X、Y的硝酸盐溶液中 | 铁片表面附着红色固体 | 铁片表面附着银白色固体 |
(2)取两支试管分别放入铁和金属Y,同时加入等量的稀盐酸,预期可以观察到的现象是铁和Y的表面有气泡生成,铁的表面产生的气泡快;将金属Y加入到X的硝酸盐溶液中,预期可以观察到的现象是在Y的表面有红色物质生成;
(3)现有X、Y两种金属粉末的混合物,设计实验将X和Y充分分离,写出实验操作步骤.(提示:分离混合物需加入稍过量的试剂以达到最大限度的分离)
1.工业上侯氏制碱法制得的纯碱产品中常含有少量的氯化钠杂质,化验员要对每批次的纯碱产品进行检验.在实验室中取27g纯碱样品,平均分成五份依次加入到盛有100g稀盐酸的锥形瓶中(锥形瓶的质量为60g),每次充分反应后都进行称量,得到的实验数据如表:
(1)第一次加入纯碱样品充分反应后,生成二氧化碳的质量是2.2g.
(2)第三次加入纯碱样品后恰好与100g稀盐酸完全反应,此时共反应纯碱样品16.2g.
(3)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)
| 第一次 | 第二次 | 第三次 | 第四次 | 第五次 | |
| 加入纯碱样品的质量/g | 5.4 | 5.4 | 5.4 | 5.4 | 5.4 |
| 电子天平的示数/g | 163.2 | 166.4 | 169.6 | 175 | 180.4 |
(2)第三次加入纯碱样品后恰好与100g稀盐酸完全反应,此时共反应纯碱样品16.2g.
(3)计算纯碱样品中碳酸钠的质量分数是多少?(计算结果精确到0.1%)