题目内容
9.一定量的碳和氧气放入一密闭容器中燃烧,待氧气耗尽时,得到5g气体.将该气体通过足量石灰水后,气体剩余2.8g.试计算反应前密闭容器中氧气的质量.分析 碳在和氧气反应时存在两种情况,在氧气充足时生成二氧化碳,在氧气不足时反应生成一氧化碳,根据题意可以知道,氧气已被完全消耗,所以将气体通入石灰水后剩余的气体为一氧化碳,那么生成的二氧化碳的气体的质量为5g-2.8g=2.2g,可以据此结合反应的化学方程式求算出氧气的质量.
解答 解:设生成8.8g二氧化碳需要氧气的质量为x
C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
32 44
x 2.2g
$\frac{32}{x}=\frac{44}{2.2g}$
解得:x=1.6g
设生成2.8g一氧化碳需要氧气的质量为y
2C+O2$\frac{\underline{\;点燃\;}}{\;}$2CO
32 56
y 2.8g
$\frac{32}{y}=\frac{56}{2.8g}$
解得:y=1.6g
所以碳在发生完全燃烧和不完全燃烧的过程中共消耗氧气的质量为:1.6g+1.6g=3.2g
答案:反应前密闭容器中氧气的质量为3.2g
点评 本题主要考查碳单质和氧气的反应情况,氧气量充足和不足会导致产物有所不同是解题的关键所在.

练习册系列答案
相关题目
19.下列实验操作中,正确的是( )
| A. |  过滤 | B. |  称取氯化钠 称取氯化钠 | C. |  稀释浓硫酸 | D. |  测溶液的pH |
17.实验室用氯酸钾和二氧化锰制氧气,有以下操作:(1)加热(2)检查装置的气密性(3)装药(4)用排水集气法收集气体(5)从水槽中取出导管(6)熄灭酒精灯(7)连接仪器,正确的顺序是( )
| A. | (7)(2)(3)(1)(4)(5)(6) | B. | (7)(2)(3)(1)(4)(6)(5) | C. | (7)(3)(2)(1)(4)(5)(6) | D. | (7)(3)(2)(1)(4)(6)(5) |
4.一氧化碳中混有少量二氧化碳,除去二氧化碳的方法是( )
| A. | 将气体通过灼热的氧化铜 | B. | 将气体通入足量的澄清石灰水中 | ||
| C. | 将气体点燃 | D. | 倾倒,将上层的二氧化碳倒出 |
14.欲证明生石灰中含有石灰石,最简单的方法是( )
| A. | 加热 | B. | 加水,通入CO2 | C. | 高温煅烧 | D. | 滴加稀盐酸 |
1.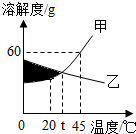 如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
 如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )
如图是甲、乙两种固体物质的溶解度曲线.下列说法正确的是( )| A. | 甲物质的溶解度为60g | |
| B. | 阴影部分各点对应的溶液(不包括曲线上的点)是甲的不饱和溶液,乙的饱和溶液 | |
| C. | 升高温度可使不饱和的甲溶液变为饱和 | |
| D. | 45℃时,两物质各10克分别加水至恰好溶解,所得饱和溶液质量是甲小于乙 |
 根据如图中a、b、c三种物质的溶解度曲线,回答下列问题:
根据如图中a、b、c三种物质的溶解度曲线,回答下列问题: