题目内容
4.2017年5月,我国首次海域可燃冰试采成功,可燃冰外观像冰,主要含有甲烷水合物(由甲烷分子和水分子组成),还含少量二氧化碳等物质.(1)可燃冰属于混合物(填“纯净物”或“混合物”).
(2)化学家在较低的温度和压力下,用甲烷等为原料制成了金刚石薄膜,该变化属于化学变化(填“物理变化”或‘化学变化”).
(3)甲烷(CH4)可用作燃料,其充分燃烧的化学方程式为CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(4)常温常压时,由甲烷和另两种气体组成的混合物中,碳元素的质量分数为80%,则另两种气体可能是BCD.
A.H2和CO B.H2和C2H2C.C2H2和C2H4D.CO和C2H4.
分析 (1)根据可燃冰的组成分析回答;
(2)根据化学变化与物理变化的本质区别进行解答;
(3)根据甲烷燃烧生成二氧化碳和水分析解答;
(4)根据物质中某元素的质量分数计算方法进行解答.
解答 解:(1)“可燃冰”是甲烷和水在低温、高压条件下形成的一种比较复杂的固体混合物,能够燃烧,外形和冰相似,又称为可燃冰;
(2)用甲烷等为原料制成金刚石薄膜的过程中有新物质生成,属于化学变化;
(3)甲烷充分燃烧生成二氧化碳和水,反应的化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O;
(4)甲烷中,碳元素的质量百分比=$\frac{12×1}{12×1+1×4}$×100%=75%,
CO中碳元素的质量百分比=$\frac{12}{12+16}$×100%=42.9%;
C2H2中碳元素的质量百分比=$\frac{12×2}{12×2+1×2}$×100%=92.3%
C2H4中碳元素的质量百分比=$\frac{12×2}{12×2+1×4}$×100%=85.7%
因为混合气体的碳元素质量分数为80%,而甲烷<80%,所以,另两种气体的含碳量一定要>80% 才能使混合气体中碳元素质量分数达到80%,A中H2和CO达不到要求,B中H2和C2H2,C中C2H2和C2H4,D中CO和C2H4;都可以达到要求;
故答案为:(1)混合物;(2)化学变化;(3)CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O; (4)BCD.
点评 化学来源于生产生活,也必须服务于生产生活,所以与人类生产生活相关的化学知识也是重要的中考热点之一.

练习册系列答案
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案
相关题目
14.下列叙述正确的是( )
| A. | 催化剂是能改变化学反应速率而本身的质量和性质都不变的物质 | |
| B. | 氢、碳、氧的原子核都由质子和中子构成 | |
| C. | pH=0的溶液呈中性 | |
| D. | 饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液 |
15.实验室有一瓶碳酸钙和氯化钙粉末组成的均匀混合物,小科用相同溶质质量分数的稀盐酸和该混合物反应(所得溶液均为不饱和溶液),四组实验数据记录如表,请分析计算:
(1)反应后,稀盐酸还有剩余的是第一、二组;
(2)求混合物中碳酸钙和氯化钙质量之比;
(3)表中a的值为105.5;
(4)求表中m的值.
| 实验组别 | 一 | 二 | 三 | 四 |
| 稀盐酸质量/g | 100.0 | 100.0 | 100.0 | 100.0 |
| 混合物质量/g | 3.0 | 6.0 | 9.0 | 12.0 |
| 所得溶液质量/g | 101.9 | 103.8 | 105.0 | a |
| 剩余固体质量/g | 0 | 0 | m | n |
(2)求混合物中碳酸钙和氯化钙质量之比;
(3)表中a的值为105.5;
(4)求表中m的值.
12.下列除杂所选用试剂与操作方法均正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂试剂 | 实验操作 |
| A | CaO(CaCO3) | 水 | 溶解、过滤 |
| B | H2(CO) | 灼热CuO | 洗气 |
| C | NaCl(Na2SO4) | 过量BaCl2溶液 | 过滤 |
| D | NaCl(Na2CO3) | 足量稀盐酸 | 蒸发结晶 |
| A. | A | B. | B | C. | C | D. | D |
9.下列图象能正确反映其对应操作的是( )
| A. | 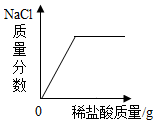 一定量的NaOH溶液中逐滴加入稀盐酸 | |
| B. | 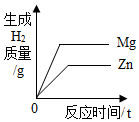 等质量、等质量分数的稀硫酸中分别加入足量的镁粉和锌粉 | |
| C. | 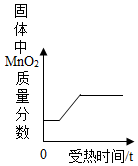 用适量KClO3和MnO2的混合物加热制取O2 | |
| D. | 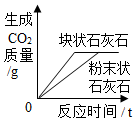 等质量、不同形状的石灰石中分別加入足量相同的稀盐酸 |
16.郴州是温泉之乡,温泉水中溶解了多种矿物质.下列有关水的说法错误的时( )
| A. | 可用肥皂水检验泉水是否属于硬水 | |
| B. | 温泉水是纯净水 | |
| C. | 活性炭可吸附水中的色素和有异味的物质 | |
| D. | 水能溶解很多种物质,是一种最常用的溶剂 |
14.下列关于金属的说法中,不正确的是( )
| A. | 铜有良好的导电性,常用于制作导线 | |
| B. | 所有的金属都能与稀盐酸反应 | |
| C. | 铁制品在干燥的空气中不易生锈 | |
| D. | 不锈钢具有较强的耐腐蚀性,可用于制作医疗器械 |