题目内容
请你参与某学习小组进行研究性学习的过程,并协助完成相关任务.小华同学向一定量的纯碱溶液中投入一定量的生石灰,充分反应,冷却到常温后,观察到有白色不溶物,过滤,得滤液A和白色固体B.
写出上述实验中有关的化学方程式:,.
【问题】滤液成分是什么?白色固体的成分是什么?
【猜想】请补充完成下列猜想.
| 猜想 | (1) | (2) | (3) | (4) |
| 溶液A的溶质 | NaOH | NaOH Na2CO3 | NaOH Ca(OH)2 | |
| 白色固体B的成分 | CaCO3 | CaCO3 | CaCO3 Ca(OH)2 |
| 实验步骤 | 实验现象 | 实验结论 |
| 溶液A的溶质是 NaOH和Na2CO3 |
【答案】分析:给出一个实验探究题,应首先分析所给物质发生的反应,写全其中所有的化学方程式.然后根据科学探究的步骤:提出问题、猜想假设、设计实验方案、进行试验、得出结论、反思评价等来完成题目.其中在猜想反应后剩余物质成分是要根据反应物完全反应和有一种反应物剩余两种情况来考虑.
解答:解:纯碱溶液中投入一定量的生石灰,发生的反应有:首先生石灰氧化钙和水反应生成氢氧化钙,其次氢氧化钙和纯碱碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
滤液成分是什么?白色固体的成分是什么?这两句话显然是提出的问题;
下面应该猜想滤滤液液A中的溶质和白色固体B的成分,因为NaOH和CaCO3是生成物,所以滤液A中肯定有NaOH,而白色固体B中肯定有CaCO3.(1)如果Na2CO3和Ca(OH)2恰好完全反应,那么滤液A中只有NaOH,而白色固体B中只有CaCO3;(2)如果纯碱溶液有剩余,那么滤液A中除NaOH外还有Na2CO3,白色固体B中只有CaCO3;(3)如果氢氧化钙有剩余,那么分两种情况,一种是氢氧化钙剩余的不太多,只在溶液中有,那么滤液A有NaOH和Ca(OH)2,白色固体B中是CaCO3;还有一种情况是(4)氢氧化钙剩余量比较大,而氢氧化钙是微溶的,剩余溶解不了的氢氧化钙就会作为沉淀析出,所以滤液A中有NaOH和Ca(OH)2,而白色固体B中有CaCO3和Ca(OH)2.
下面要设计滤液A的实验证明猜想(2)是正确的,因为猜想(2)的滤液中含有的溶质是氢氧化钠和碳酸钠,所以可以先加过量的氯化钡或氯化钙,若有沉淀生成证明含有碳酸钠,然后过滤后再向滤液中滴加酚酞试液,若酚酞变红,证明有氢氧化钠存在.
故答案为:
CaO+H2O═Ca(OH)2,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
问题,猜想,(4)NaOH、Ca(OH)2 (2)CaCO3;
实验步骤:取滤液A少量于试管中,向其中加入过量的BaCl2溶液;过滤后再向滤液中加入几滴酚酞试液.
实验现象:产生白色沉淀,溶液变为红色.
点评:此题是一道较难的实验探究题.其中难点之一是4种猜想,大部分同学会猜想出前三种而卡在第四种上;难点之二是实验步骤那里用氯化钡而不要用氢氧化钡,用氢氧化钡虽然能判断出碳酸钠的存在,但由于引入了氢氧根而无法判断氢氧化钠的存在,同学们往往容易忽视这一点.
解答:解:纯碱溶液中投入一定量的生石灰,发生的反应有:首先生石灰氧化钙和水反应生成氢氧化钙,其次氢氧化钙和纯碱碳酸钠反应生成碳酸钙沉淀和氢氧化钠;
滤液成分是什么?白色固体的成分是什么?这两句话显然是提出的问题;
下面应该猜想滤滤液液A中的溶质和白色固体B的成分,因为NaOH和CaCO3是生成物,所以滤液A中肯定有NaOH,而白色固体B中肯定有CaCO3.(1)如果Na2CO3和Ca(OH)2恰好完全反应,那么滤液A中只有NaOH,而白色固体B中只有CaCO3;(2)如果纯碱溶液有剩余,那么滤液A中除NaOH外还有Na2CO3,白色固体B中只有CaCO3;(3)如果氢氧化钙有剩余,那么分两种情况,一种是氢氧化钙剩余的不太多,只在溶液中有,那么滤液A有NaOH和Ca(OH)2,白色固体B中是CaCO3;还有一种情况是(4)氢氧化钙剩余量比较大,而氢氧化钙是微溶的,剩余溶解不了的氢氧化钙就会作为沉淀析出,所以滤液A中有NaOH和Ca(OH)2,而白色固体B中有CaCO3和Ca(OH)2.
下面要设计滤液A的实验证明猜想(2)是正确的,因为猜想(2)的滤液中含有的溶质是氢氧化钠和碳酸钠,所以可以先加过量的氯化钡或氯化钙,若有沉淀生成证明含有碳酸钠,然后过滤后再向滤液中滴加酚酞试液,若酚酞变红,证明有氢氧化钠存在.
故答案为:
CaO+H2O═Ca(OH)2,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH;
问题,猜想,(4)NaOH、Ca(OH)2 (2)CaCO3;
实验步骤:取滤液A少量于试管中,向其中加入过量的BaCl2溶液;过滤后再向滤液中加入几滴酚酞试液.
实验现象:产生白色沉淀,溶液变为红色.
点评:此题是一道较难的实验探究题.其中难点之一是4种猜想,大部分同学会猜想出前三种而卡在第四种上;难点之二是实验步骤那里用氯化钡而不要用氢氧化钡,用氢氧化钡虽然能判断出碳酸钠的存在,但由于引入了氢氧根而无法判断氢氧化钠的存在,同学们往往容易忽视这一点.

练习册系列答案
相关题目
下面是某实验小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.
研究课题:探究草酸晶体受热分解的产物
查阅资料:
(1)该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
(2)白色的无水硫酸铜遇水蒸气会变蓝色
作出猜想:
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是 、 (你猜想的产物化学式)
设计实验:

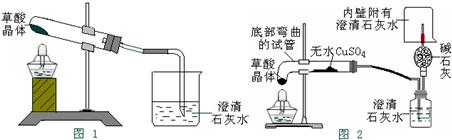
实验操作:甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有 ; 无水CuSO4变蓝,证明产物中还有 若产物中有CO,则乙的对应实验现象是 证明CO生成的化学反应方程式是 、 .
得出结论:若第二种猜想是正确的,请你写出草酸分解的反应方程式 .
反思评价:乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点: ;
.
利用乙设计的装置证明产物中没有H2的方法是: .
交流讨论:丙同学继续查阅相关资料发现:草酸是一种酸,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色不溶物.丙同学通过进一步研究,对实验中CO2的检验提出质疑,并提出实验的改进措施,他提出的措施是 .
研究课题:探究草酸晶体受热分解的产物
查阅资料:
(1)该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
| 名称 | 化学式 | 颜色、状态 | 溶解性 | 熔点(℃) | 密度(g/cm3) | 草酸 | H2C2O4 | - | 易溶于水 | 189.5 | 1.900 | 草酸晶体 | H2C2O4?2H2O | 无色晶体 | - | 101.5 | 1.650 |
作出猜想:
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是
设计实验:

实验操作:甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有
得出结论:若第二种猜想是正确的,请你写出草酸分解的反应方程式
反思评价:乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:
利用乙设计的装置证明产物中没有H2的方法是:
交流讨论:丙同学继续查阅相关资料发现:草酸是一种酸,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色不溶物.丙同学通过进一步研究,对实验中CO2的检验提出质疑,并提出实验的改进措施,他提出的措施是
下面是某实验小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.
研究课题:探究草酸晶体受热分解的产物
查阅资料:
(1)该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
(2)白色的无水硫酸铜遇水蒸气会变蓝色
作出猜想:
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
设计实验:
实验操作:甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了;乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有 ; 无水CuSO4变蓝,证明产物中还有 若产物中有CO,则乙的对应实验现象是 证明CO生成的化学反应方程式是 、
得出结论:若第二种猜想是正确的,请你写出草酸分解的反应方程式 .
反思评价:乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:
1 ;2 .

研究课题:探究草酸晶体受热分解的产物
查阅资料:
(1)该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
| 名称 | 化学式 | 颜色、状态 | 溶解性 | 熔点(℃) | 密度(g/cm3) |
| 草酸 | H2C2O4 | - | 易溶于水 | 189.5 | 1.900 |
| 草酸晶体 | H2C2O4?2H2O | 无色晶体 | - | 101.5 | 1.650 |
作出猜想:
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
设计实验:
实验操作:甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了;乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有 ; 无水CuSO4变蓝,证明产物中还有 若产物中有CO,则乙的对应实验现象是 证明CO生成的化学反应方程式是 、
得出结论:若第二种猜想是正确的,请你写出草酸分解的反应方程式 .
反思评价:乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:
1 ;2 .

下面是某实验小组的同学进行研究性学习的过程,请你参与并协助他们完成相关学习任务.
研究课题:探究草酸晶体受热分解的产物
查阅资料:
(1)该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
(2)白色的无水硫酸铜遇水蒸气会变蓝色
作出猜想:
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是、(你猜想的产物化学式)
设计实验:

实验操作:甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有; 无水CuSO4变蓝,证明产物中还有若产物中有CO,则乙的对应实验现象是证明CO生成的化学反应方程式是、.
得出结论:若第二种猜想是正确的,请你写出草酸分解的反应方程式.
反思评价:乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:;
.
利用乙设计的装置证明产物中没有H2的方法是:.
交流讨论:丙同学继续查阅相关资料发现:草酸是一种酸,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色不溶物.丙同学通过进一步研究,对实验中CO2的检验提出质疑,并提出实验的改进措施,他提出的措施是.
研究课题:探究草酸晶体受热分解的产物
查阅资料:
(1)该小组同学通过网络查询,获得草酸及草酸晶体的一些相关知识:
| 名称 | 化学式 | 颜色、状态 | 溶解性 | 熔点(℃) | 密度(g/cm3) |
| 草酸 | H2C2O4 | - | 易溶于水 | 189.5 | 1.900 |
| 草酸晶体 | H2C2O4?2H2O | 无色晶体 | - | 101.5 | 1.650 |
作出猜想:
第一种:草酸分解产物CO2和H2
第二种:草酸分解产物是CO2、CO和H2O
第三种:草酸的分解产物是、(你猜想的产物化学式)
设计实验:

实验操作:甲同学按其设计的实验装置(如图1)实验时观察到澄清的石灰水变浑浊了乙同学按图2的装置实验也观察到澄清的石灰水变浑浊了,这些现象证明产物中一定有; 无水CuSO4变蓝,证明产物中还有若产物中有CO,则乙的对应实验现象是证明CO生成的化学反应方程式是、.
得出结论:若第二种猜想是正确的,请你写出草酸分解的反应方程式.
反思评价:乙认为甲设计的实验装置有缺陷:由于试管口向下倾斜,草酸晶体熔点较低,加热到182℃便开始熔化,因此实验中会出现熔融的草酸流进导管而影响后续实验.请你谈谈装置2的至少两点优于装置1的优点:;
.
利用乙设计的装置证明产物中没有H2的方法是:.
交流讨论:丙同学继续查阅相关资料发现:草酸是一种酸,在受热分解过程中有少量升华;草酸钙和草酸氢钙均为白色不溶物.丙同学通过进一步研究,对实验中CO2的检验提出质疑,并提出实验的改进措施,他提出的措施是.