题目内容
9.根据题目要求填空| 实验内容 | 实验现象 | 反应的文字表达式 |
| 硫在空气中燃烧 | ||
| 磷在空气中燃烧 | ||
| 铝箔在氧气中燃烧 | ||
| 铁丝在氧气中燃烧 |
分析 首先根据反应原理找出反应物、生成物、反应条件,根据文字表达式的书写方法、步骤进行书写;根据硫、铁丝在氧气中燃烧的现象进行分析解答即可.
解答 解:(1)硫在氧气中燃烧,发出明亮的蓝紫色火焰,放出热量,产生一种具有刺激性气味的气体;硫在氧气中燃烧生成二氧化硫,反应的文字表达式为:硫+氧气$\stackrel{点燃}{→}$二氧化硫;
(2)磷在空气中燃烧,发出黄色火焰,产生大量白烟,放出热量,反应的文字表达式为:磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)铝箔在氧气中燃烧,剧烈燃烧,发出耀眼的白光,放出热量,生成白色固体.反应的文字表达式为:铝+氧气$\stackrel{点燃}{→}$氧化铝.
(4)铁丝在氧气中剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体;铁丝在氧气中燃烧生成四氧化三铁,反应的文字表达式为:铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
故答案为:(1)发出明亮的蓝紫色火焰,放出热量,产生一种具有刺激性气味的气体;硫+氧气$\stackrel{点燃}{→}$二氧化硫;
(2)能燃烧,发出黄色火焰,产生大量白烟,放出热量.磷+氧气$\stackrel{点燃}{→}$五氧化二磷.
(3)剧烈燃烧,发出耀眼的白光,放出热量,生成白色固体.铝+氧气$\stackrel{点燃}{→}$氧化铝.
(4)剧烈燃烧,火星四射,放出大量的热,生成一种黑色固体;铁+氧气$\stackrel{点燃}{→}$四氧化三铁.
点评 本题难度不大,掌握常见物质燃烧的现象、文字表达式的书写方法即可正确解答本题.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
20.重水的是在核反应堆中作减速剂,一个重水分子由2个重氢原子和1个氧原子构成.重氢原子核电荷数为1,相对原子质量为2,下列说法正确的是( )
| A. | 重氢原子核内有1个质子 | B. | 重氢原子核外有2个电子 | ||
| C. | 重氢原子核内没有中子 | D. | 重氢原子核内有2个质子 |
17.在一密闭容器内加入甲、乙、丙、丁四种物质,在一定条件下发生化学反应,反应前后各物质的质量变化见下表.下列说法中正确的是( )
| 物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前物质质量/g | 8 | 32 | x | 4 |
| 反应后物质质量/g | 16 | 4 | 待测 | 24 |
| A. | 该反应为化合反应 | |
| B. | 丙一定为该反应的催化剂 | |
| C. | 待测值一定是4g | |
| D. | 甲、丁两种物质间反应的质量比为2:5 |
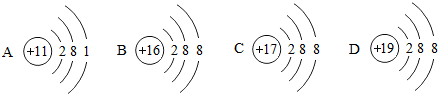
18.如图,这四位同学描述的可能同是下面的哪一个化学符号( )

| A. | SO2 | B. | O2 | C. | CO | D. | OH- |
19.牙膏是生活中常见的物质,其配料成分有摩擦剂、增稠剂、发泡剂等,其中摩擦剂的类型有很多,如CaCO3、Al(OH)3、SiO2或这些物质的混合物.我校化学兴趣小组同学想研究牙膏摩擦剂的成分.
[实验探究一]某品牌牙膏中是否含有CaCO3?
[查阅资料]二氧化硅不与稀盐酸反应
[实验方案]
[实验探究二]该牙膏中CaCO3的含量是多少?
[实验装置]利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

[友情提示]
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
[实验步骤]
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置C,打开K1,关闭K2,通入空气一段时间,目的是排除装置内的空气
--,再接上装置C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再
打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将留在装置内的二氧化碳排到装置C中;
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
[实验数据]重复实验,3次数据记录如下:
[实验分析及数据处理]
(1)装置A的作用是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳进入到装置C内,产生误差.
(4)据上表数据,取C装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量,然后可求出牙膏样品中CaCO3的质量分数为25%.

[实验探究一]某品牌牙膏中是否含有CaCO3?
[查阅资料]二氧化硅不与稀盐酸反应
[实验方案]
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,滴加稀盐酸; | ①产生气泡 | 该牙膏样品中含有CaCO3 |
| ②将产生的气体通入澄清的石灰水中 | ②石灰水变浑浊 |
[实验装置]利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

[友情提示]
(1)氢氧化钡跟氢氧化钙的性质类似,CO2+Ba(OH)2═BaCO3↓+H2O;
(2)CO2的相对分子质量为44,CaCO3的相对分子质量为100,BaCO3的相对分子质量为197;
(3)以上药品均足量,且每步反应或作用都是完全的.
[实验步骤]
(1)按上图连接好装置后,检查装置的气密性;
(2)在B装置中加入牙膏样品8.00g;
(3)先断开装置C,打开K1,关闭K2,通入空气一段时间,目的是排除装置内的空气
--,再接上装置C;关闭K1,打开K2(选填“打开”或“关闭”),向牙膏样品中滴入10%的盐酸,至不再产生气泡为止,停止滴加盐酸;然后再
打开K1,关闭K2(选填“打开”或“关闭”),缓缓通入空气至C中不再产生沉淀为止,目的是将留在装置内的二氧化碳排到装置C中;
(4)将C装置中的固液混合物过滤、洗涤、烘干后称量其质量;
(5)重复实验.
[实验数据]重复实验,3次数据记录如下:
| 实验次数 | 实验1 | 实验2 | 实验3 |
| C装置中沉淀质量(g) | 3.93 | 3.94 | 3.95 |
(1)装置A的作用是2NaOH+CO2=Na2CO3+H2O(用化学方程式表示),若没有A装置,则测定结果将偏大(选填“偏大”、“偏小”或“不变”).
(2)装置B中产生气体的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)装置D的作用是防止空气中的二氧化碳进入到装置C内,产生误差.
(4)据上表数据,取C装置中沉淀质量的平均值为3.94g,目的是减小偶然误差,使实验数据更准确;由产生沉淀的质量可计算出反应生成二氧化碳的质量,然后可求出牙膏样品中CaCO3的质量分数为25%.
 元素周期表是学习和研究化学的重要工具.回答下列问题:
元素周期表是学习和研究化学的重要工具.回答下列问题: