题目内容
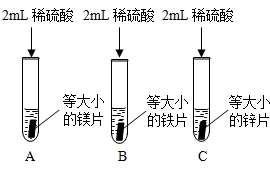 某实脸小组对实验室制取氢气的反应原理进行探究.
某实脸小组对实验室制取氢气的反应原理进行探究.【知识回顾】能产生氢气的化学反应有:①水电解②活泼金属与酸反应
【讨论交流】反应①中的化学方程式为
【实验探究】为了探究哪种物质更适合用于实脸室制取氢气,大家设计了如下实脸:
【分析与结论】填写实验报告.
| 实验序号 | 实验现象 | 实验结论 |
| A | 剧烈反应,急速产生大量气泡,试管外壁 | 反应速率过快,气体不便收集,不适用于实验室制取氢气 |
| B | 缓慢,产生大量气泡 | 反应速率过慢,不适用于实验室制取氢气 |
| C | 较快,产生大量气泡,试管外壁发热 |
【知识拓展】(1)在确定实验室制取气体的反应原理时,要考虑诸多因素,如反应的快慢、收集的难易、
(3)用稀盐酸代替稀硫酸制取氢气时.制得的气体中可能会增加的杂质为
考点:制取气体的反应原理的探究,氢气的制取和检验,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:【讨论交流】水在通电的条件下分解为氢气和氧气;
【分析与结论】金属与酸发生的置换反应要放出热量;通过比较分析出锌与酸反应的速率快慢适中,适合在实验室中制取氢气;
【知识拓展】在确定实验反应原理时:要从原理是否科学、严谨、合理,装置和操作是否安全、简便、现象明显,药品是否易得、经济、环保节能等方面进行;
盐酸具有挥发性.
【分析与结论】金属与酸发生的置换反应要放出热量;通过比较分析出锌与酸反应的速率快慢适中,适合在实验室中制取氢气;
【知识拓展】在确定实验反应原理时:要从原理是否科学、严谨、合理,装置和操作是否安全、简便、现象明显,药品是否易得、经济、环保节能等方面进行;
盐酸具有挥发性.
解答:解:【交流讨论】水在通电的条件下分解为氢气和氧气,化学方程式为:2H2O
2H2↑+O2↑;故填:2H2O
2H2↑+O2↑;
【分析与结论】镁与稀硫酸反应速率较快,放出热量,感觉试管外壁发烫,锌与稀硫酸反应产生气泡的速率较快,便于在实验室中制取氢气;锌与硫酸反应生成硫酸锌和氢气;故填:
Zn+H2SO4=ZnSO4+H2↑;
【知识拓展】(1)在确定实验反应原理时:要从原理是否科学、严谨、合理,装置和操作是否安全、简便、现象明显,药品是否易得、经济、环保节能等方面进行,故填:反应条件(或成本、气体纯度)(其他合理答案均可);
(2)盐酸具有挥发性,如果用稀盐酸代替稀硫酸制取氢气时,反应发热,会导致制取的氢气中混有氯化氢气体.故填:氯化氢.
| ||
| ||
【分析与结论】镁与稀硫酸反应速率较快,放出热量,感觉试管外壁发烫,锌与稀硫酸反应产生气泡的速率较快,便于在实验室中制取氢气;锌与硫酸反应生成硫酸锌和氢气;故填:
| 实验序号 | 实验现象 | 实验结论 |
| A | 剧烈反应,急速产生大量气泡,试管外壁 发烫 | 反应速率过快,气体不便收集,不适用于实验室制取氢气 |
| B | 缓慢,产生大量气泡 | 反应速率过慢,不适用于实验室制取氢气 |
| C | 较快,产生大量气泡,试管外壁发热 | 反应速率适中,适用于实验室制取氢气 |
【知识拓展】(1)在确定实验反应原理时:要从原理是否科学、严谨、合理,装置和操作是否安全、简便、现象明显,药品是否易得、经济、环保节能等方面进行,故填:反应条件(或成本、气体纯度)(其他合理答案均可);
(2)盐酸具有挥发性,如果用稀盐酸代替稀硫酸制取氢气时,反应发热,会导致制取的氢气中混有氯化氢气体.故填:氯化氢.
点评:本题考查学生根据盐酸挥具有挥发性,实验室制取气体的反应原理进行分析解题的能力.

练习册系列答案
相关题目
鉴别下列各组物质所用的方法或试剂,错误的是( )
| A、氧气与氨气---带火星的木条 |
| B、二氧化碳与一氧化碳---闻气味 |
| C、氯化铵与氯化钾---用熟石灰 |
| D、二氧化锰与氧化铜---用稀硫酸 |
不属于碳元素的同素异形体的是( )
| A、金刚石 | B、石墨 |
| C、碳60 | D、一氧化碳 |
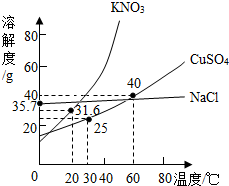 如图是几种盐的溶解度曲线,下列说法正确的是( )
如图是几种盐的溶解度曲线,下列说法正确的是( )| A、40℃时将35gNaCl溶 于100g水中,降温至0℃时,可析出NaCl晶体 |
| B、20℃时KNO3饱和溶液的质量分数是31.6% |
| C、60℃时,200g水中溶解80gCuSO4达饱和,当降至30℃时,可析出30gCuSO4晶体 |
| D、30℃时,将35g KNO3和35gNaCl同时溶于100g水中,蒸发时先析出的是NaCl |
下列变化不能一步实现的是( )
| A、CO2→CO |
| B、Fe2O3→FeCl2 |
| C、Cu→Cu(NO3)2 |
| D、Na2CO3→NaOH |
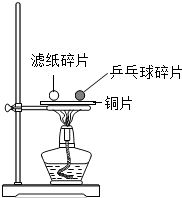 增强安全意识是我们大家共同关注的问题.
增强安全意识是我们大家共同关注的问题. 某学校化学兴趣小组的同学想测定赤铁矿中氧化铁的含量,做了如下实验:首先称取100g该赤铁矿样品放入烧杯中,然后将500g的稀盐酸分5次加入烧杯内(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下:
某学校化学兴趣小组的同学想测定赤铁矿中氧化铁的含量,做了如下实验:首先称取100g该赤铁矿样品放入烧杯中,然后将500g的稀盐酸分5次加入烧杯内(假设其余杂质均不与盐酸反应也不溶于水)进行充分反应.实验过程中的数据记录如下: