题目内容
小宇同学将18g高锰酸钾放在试管里加热制取氧气,反应一段时间后,称量试管内剩余固体的质量为16.4g.
(1)计算高锰酸钾分解后产生氧气的质量;
(2)高锰酸钾的分解率是多少?
(1)计算高锰酸钾分解后产生氧气的质量;
(2)高锰酸钾的分解率是多少?
考点:根据化学反应方程式的计算
专题:有关化学方程式的计算
分析:根据质量守恒定律,试管内质量的减少的质量即生成的氧气质量,据此根据反应的化学方程式列式计算出参加反应的高锰酸钾的质量,进而计算出高锰酸钾的分解率.
解答:解:(1)由质量守恒定律,生成氧气的质量为18g-16.4g=1.6g.
(2)设参加反应的高锰酸钾的质量为x
2KMnO4
K2MnO4+MnO2+O2↑
316 32
x 1.6g
=
x=15.8g
高锰酸钾的分解率是
×100%≈87.8%.
答:(1)计算高锰酸钾分解后产生氧气的质量为1.6g;(2)高锰酸钾的分解率是87.8%.
(2)设参加反应的高锰酸钾的质量为x
2KMnO4
| ||
316 32
x 1.6g
| 316 |
| 32 |
| x |
| 1.6g |
高锰酸钾的分解率是
| 15.8g |
| 18g |
答:(1)计算高锰酸钾分解后产生氧气的质量为1.6g;(2)高锰酸钾的分解率是87.8%.
点评:本题难度不大,掌握根据化学方程式的计算即可正确解答本题,根据质量守恒定律计算出氧气的质量是正确解答本题的前提和关键.

练习册系列答案
 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案 全程金卷系列答案
全程金卷系列答案
相关题目
下列过程中没有发生化学变化的是( )
| A、燃放礼花 | B、面包变质 |
| C、植物光合作用 | D、菠萝榨汁 |
对有关空气和水资源的叙述中,错误的是( )
| A、利用空气资源,在工业上将其发生分解反应来制取氧气 |
| B、地球上水的总储量很大,但淡水资源并不充裕 |
| C、缺水会造成土壤沙漠化,土壤沙漠化也会引发空气污染 |
| D、海洋不属于淡水资源,但却蕴藏着大量的化学资源 |
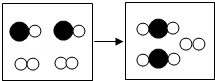 如图是某化学反应的微观示意图.“
如图是某化学反应的微观示意图.“ ”和“
”和“ ”分别表示不同的原子.
”分别表示不同的原子.