题目内容
19.小强向一定量的AgNO3和Cu(NO3)2混合溶液加入一定量的锌粉,并对过滤后得到的溶液A和固体B的成分进行分析和研究.(1)由推理可知:溶液A中的一定含有的溶质是Zn(NO3)2(填化学式)
写出一个你认为已发生的化学反应方程式:Zn+2AgNO3=Zn(NO3)2+2Ag.
(2)小强将固体B洗净,通过以下实验确定其成分,请将下表填写完整.
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加稀盐酸或稀硫酸 | 有较多气泡产生 | 固体B含有Zn、Ag、Cu |
分析 锌比铜活泼,铜比银活泼;
锌和硝酸银反应生成硝酸锌和银,和硝酸铜反应生成硝酸锌和铜;
锌和稀盐酸或稀硫酸反应生成氯化锌或硫酸锌和氢气.
解答 解:(1)向一定量的AgNO3和Cu(NO3)2混合溶液加入一定量的锌粉,锌先和硝酸银反应生成硝酸锌和银,因此溶液A中的一定含有的溶质是Zn(NO3)2.
故填:Zn(NO3)2.
因为向一定量的AgNO3和Cu(NO3)2混合溶液加入一定量的锌粉,锌先和硝酸银反应生成硝酸锌和银,因此一定发生的反应是锌和硝酸银反应生成硝酸锌和银,反应的化学方程式为:.
故填:Zn+2AgNO3=Zn(NO3)2+2Ag.
(2)小强将固体B洗净,通过以下实验确定其成分,实验过程如下表所示:
| 实验步骤 | 现象 | 实验结论 |
| 取少量固体B,滴加稀盐酸或稀硫酸 | 有较多气泡产生 | 固体B含有Zn、Ag、Cu |
故填:AgNO3、Cu(NO3)2.
点评 要会利用金属活动顺序表分析实验,氢前边的金属会与稀硫酸、盐酸反应,但氢后边的金属不会与稀硫酸、盐酸反应,前边的金属会把后边的金属从其盐溶液中置换出来.

练习册系列答案
相关题目
7.下列物质由原子构成的是( )
| A. | 铜 | B. | 氧气 | C. | 水 | D. | 氯化钠 |
14.分别将下列各组物质同时加入水中,仅得到无色透明溶液的是( )
| A. | HCl Na2SO4 KCl | B. | K2SO4 HCl Ba(OH)2 | ||
| C. | NaCl BaCO3 KNO3 | D. | FeCl3 KOH NaCl |
8.只能表示2个氢原子的化学符号是( )
| A. | H2O | B. | H | C. | H2 | D. | 2H |
4.下列物质中,由分子构成的是( )
| A. | 烧碱 | B. | 金刚石 | C. | 氯化钠 | D. | 酒精 |
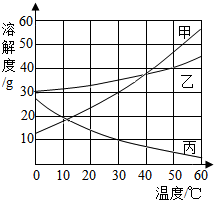 甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题:
甲、乙、丙三种物质的溶解度曲线如图所示.根据图中信息回答下列问题:
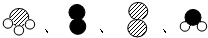 四种粒子的个数比是4:3:2:6.
四种粒子的个数比是4:3:2:6.