题目内容
 化学兴趣小组的同学用如图所示装置做中和反应实验,请按要求回答问题.
化学兴趣小组的同学用如图所示装置做中和反应实验,请按要求回答问题.(1)向盛有氢氧化钠溶液的烧杯中滴入酚酞溶液,溶液变为红色,此时溶液的pH
(2)实验(1)中,某同学又多加了几滴盐酸,这时溶液显
考点:中和反应及其应用,溶液的酸碱性与pH值的关系,书写化学方程式、文字表达式、电离方程式
专题:常见的酸 酸的通性
分析:盐酸和氢氧化钠发生的中和反应时无明显的现象,为了确定是否发生了反应,滴加酚酞试液通过颜色的改变确定是否发生了反应.当盐酸适量时,溶液颜色由红色恰好变为无色,当盐酸过量时溶液呈酸性.
解答:解:
(1)由于氢氧化钠属于碱,故其溶液显碱性,则氢氧化钠溶液中滴加酚酞溶液,溶液变红色,此时溶液的pH>7;盐酸显酸性,当滴加盐酸溶液时盐酸和氢氧化钠发生反应,当两者恰好完全反应时,溶液呈中性,溶液颜色由红色变为无色.故答案为:无;HCl+NaOH=NaCl+H2O;
(2)当滴加盐酸的量过量时,溶液呈酸性,溶液颜色不变,但pH<7,此时溶液中的溶质为HCl、NaCl、酚酞.
答案:
(1)>无 NaOH+HCl=NaCl+H2O
(2)酸; HCl、NaCl、酚酞
(1)由于氢氧化钠属于碱,故其溶液显碱性,则氢氧化钠溶液中滴加酚酞溶液,溶液变红色,此时溶液的pH>7;盐酸显酸性,当滴加盐酸溶液时盐酸和氢氧化钠发生反应,当两者恰好完全反应时,溶液呈中性,溶液颜色由红色变为无色.故答案为:无;HCl+NaOH=NaCl+H2O;
(2)当滴加盐酸的量过量时,溶液呈酸性,溶液颜色不变,但pH<7,此时溶液中的溶质为HCl、NaCl、酚酞.
答案:
(1)>无 NaOH+HCl=NaCl+H2O
(2)酸; HCl、NaCl、酚酞
点评:在中和过量的盐酸时,可用氢氧化钠也可用碳酸钠或碳酸氢钠.但不能选择其它的,因为选择其它的会引进新的杂质.

练习册系列答案
相关题目
下列有关氧气的说法正确的是( )
| A、氧气的约占空气体积的78% |
| B、硫在氧气中燃烧发出蓝紫色光 |
| C、工业分离液态空气制取氧气,是化学变化 |
| D、夏天温度升高,氧气在水中溶解度减少,鱼池内需开启增氧泵 |
4月12日,云南省保山市隆阳区永昌街道呢喃山发生森林火灾,起火原因系当地村民上坟烧纸引起.下列说法错误的是( )
| A、森林为火灾提供可燃物 |
| B、烧着的纸提高了草木的着火点 |
| C、大风为燃烧提供了充足的氧气 |
| D、用水浇是降低燃烧物的温度 |
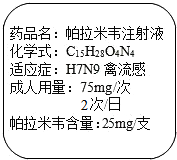 新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.
新药帕拉米韦注射液可用于治疗H7N9禽流感,其说明书中部分内容如图.