题目内容
 向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答:
向100g稀H2SO4溶液中加入一定量的镁粉,固体完全溶解后,再向所得溶液中加入质量分数为20%的NaOH溶液,所得沉淀质量与加入NaOH溶液质量关系如图所示.请回答:(1)请写出加入氢氧化钠过程当中所发生反应的化学方程式:
(2)加入镁粉的质量为
考点:根据化学反应方程式的计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据硫酸和金属镁反应生成硫酸镁和氢气,开始没有沉淀生成,说明硫酸过量,所以OA段是硫酸和NaOH溶液反应生成硫酸钠和水以及硫酸镁和氢氧化钠溶液反应生成氢氧化镁沉淀和硫酸钠进行解答;
(2)根据生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量进行解答.
(2)根据生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量进行解答.
解答:解:(1)硫酸和金属镁反应生成硫酸镁和氢气,开始没有沉淀生成,说明硫酸过量,所以OA段是硫酸和NaOH溶液反应生成硫酸钠和水以及硫酸镁和氢氧化钠溶液反应生成氢氧化镁沉淀和硫酸钠,反应的化学方程式分别为H2SO4+2NaOH=Na2SO4+2H2O、MgSO4+2NaOH═Mg(OH)2↓+Na2SO4;故填:H2SO4+2NaOH=Na2SO4+2H2O、MgSO4+2NaOH═Mg(OH)2↓+Na2SO4;
(2)生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量,由图可知生成氢氧化镁的质量为5.8g,所以加入镁粉的质量=
×100%×5.8g=2.4g;故填:2.4.
(2)生成沉淀氢氧化镁中镁元素的质量即为加入镁粉的质量,由图可知生成氢氧化镁的质量为5.8g,所以加入镁粉的质量=
| 24 |
| 24+(16+1)×2 |
点评:本题主要考查学生利用化学式进行计算的能力.解题的关键是结合物质间反应的情况,正确分析图示数据,细心解答.

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目
金属材料在生产生活中应用非常广泛,下列属于合金的是( )
| A、生铁 | B、纯铜 | C、橡胶 | D、陶瓷 |






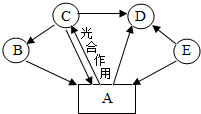 A、B、C、D、E是初中化学常见物质,转化关系如图(图中部分反应物、生成物及反应条件被省略):已知B是一种红色固体,相对分子质量为160,A能使澄清石灰水变浑浊,E是化学实验室常用燃料的主要成分,请回答下列问题:
A、B、C、D、E是初中化学常见物质,转化关系如图(图中部分反应物、生成物及反应条件被省略):已知B是一种红色固体,相对分子质量为160,A能使澄清石灰水变浑浊,E是化学实验室常用燃料的主要成分,请回答下列问题: