题目内容
元素周期表是学习化学的重要工具.下面是元素周期表中1~18号元素原子核外电子排布,我们对它进行研究: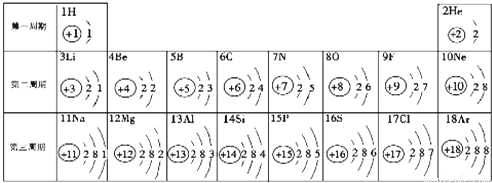
(1)第16号元素属于______元素(填“金属”或“非金属”),它在化学反应中容易______(填“得”或“失”)电子;
(2)元素的化学性质与原子结构中的______数关系密切;
(3)He与Ne、Ar原子最外层电子数不一样,但都处在每周期的最后,从原子结构上分析其原因______.
【答案】分析:(1)根据元素周期表可知,第12号元素名称、由其汉语名称可知其元素种类、由最外层电子数可知得失电子情况;
(2)元素的化合价数值一般与它的原子最外层电子数有关;或元素的化合价与该元素的离子所带的电荷数有关进行分析即可.
(3)从最外层电子数的特点分析.
解答:解:(1)根据元素周期表可知,第16号元硫元素,它属于非金属元素,它的原子的最外层有6个电子,在化学反应中容易得电子;
(2)原子在相互化合是存在得失电子或形成共用电子对,都与最外层电子数有关,所以元素的化学性质与原子的最外层电子数关系密切.
(3)He与Ne、Ar都是稀有气体元素,原子最外层电子数不一样,但最外层都是稳定结构,化学性质都不活泼,故都处在每周期的最后.
故答案为:(1)非金属;得;
(2)最外层电子
(3)最外层都是稳定结构,化学性质都不活泼.
点评:了解元素周期表的特点及其应用;核外电子在化学反应中的具体作用是解题的关键.
(2)元素的化合价数值一般与它的原子最外层电子数有关;或元素的化合价与该元素的离子所带的电荷数有关进行分析即可.
(3)从最外层电子数的特点分析.
解答:解:(1)根据元素周期表可知,第16号元硫元素,它属于非金属元素,它的原子的最外层有6个电子,在化学反应中容易得电子;
(2)原子在相互化合是存在得失电子或形成共用电子对,都与最外层电子数有关,所以元素的化学性质与原子的最外层电子数关系密切.
(3)He与Ne、Ar都是稀有气体元素,原子最外层电子数不一样,但最外层都是稳定结构,化学性质都不活泼,故都处在每周期的最后.
故答案为:(1)非金属;得;
(2)最外层电子
(3)最外层都是稳定结构,化学性质都不活泼.
点评:了解元素周期表的特点及其应用;核外电子在化学反应中的具体作用是解题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
 ,第3周期中某元素与氧元素的化学性质相似,该元素的原子结构示意图为
,第3周期中某元素与氧元素的化学性质相似,该元素的原子结构示意图为  ,则x=
,则x=
 元素周期表是学习化学的重要工具,图是元素周期表中的一格,从该图中,我们获取的相关信息中错误的是( )
元素周期表是学习化学的重要工具,图是元素周期表中的一格,从该图中,我们获取的相关信息中错误的是( ) 元素周期表是学习化学的重要工具.如图是元素周期表中的一格,从中获取的信息错误的是( )
元素周期表是学习化学的重要工具.如图是元素周期表中的一格,从中获取的信息错误的是( )