题目内容
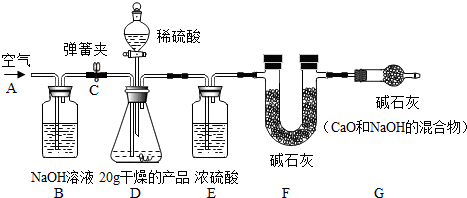
下图是某同学设计的模拟工业炼铁原理的实验装置图.请根据小资料提供的信息和下列要求回答有关问题.
(1)写出工业炼铁的化学方程式:______ 2Fe+3CO2
【答案】分析:根据已有的知识进行分析,炼铁的原理是一氧化碳与氧化铁反应生成铁和二氧化碳,浓硫酸具有吸水性,能用作干燥剂,氢氧化钠能与二氧化碳反应可用于除去二氧化碳,一氧化碳具有可燃性,是一种有毒的气体,氧化物指的是含有两种元素其中一种是氧元素的化合物.
解答:解:(1)一氧化碳能与氧化铁反应生成铁和二氧化碳,所以本题答案为:3CO+Fe2O3 2Fe+3CO2;
2Fe+3CO2;
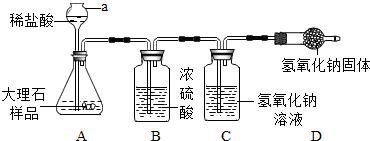
(2)浓硫酸具有吸水性,能除去一氧化碳中混有的水蒸气,氢氧化钠能与二氧化碳反应生成碳酸钠和水,
所以本题答案为:除去水蒸气,CO2+2NaOH═Na2CO3+H2O.
(3)一氧化碳有毒,能污染空气,采用燃烧的方法处理,可以节约资源,减少空气污染,所以本题答案为:充分利用资源,防止空气污染.
(4)属于氧化物额物质有一氧化碳、氧化铁、二氧化碳和水,所以本题答案为:CO、Fe2O3、CO2、H2O.
点评:本题考查了炼铁的原理以及浓硫酸和氢氧化钠的性质和氧化物的判断,完成此题,可以依据已有的知识进行,要求同学们加强基础知识的储备,以便灵活应用.
解答:解:(1)一氧化碳能与氧化铁反应生成铁和二氧化碳,所以本题答案为:3CO+Fe2O3
 2Fe+3CO2;
2Fe+3CO2;(2)浓硫酸具有吸水性,能除去一氧化碳中混有的水蒸气,氢氧化钠能与二氧化碳反应生成碳酸钠和水,
所以本题答案为:除去水蒸气,CO2+2NaOH═Na2CO3+H2O.
(3)一氧化碳有毒,能污染空气,采用燃烧的方法处理,可以节约资源,减少空气污染,所以本题答案为:充分利用资源,防止空气污染.
(4)属于氧化物额物质有一氧化碳、氧化铁、二氧化碳和水,所以本题答案为:CO、Fe2O3、CO2、H2O.
点评:本题考查了炼铁的原理以及浓硫酸和氢氧化钠的性质和氧化物的判断,完成此题,可以依据已有的知识进行,要求同学们加强基础知识的储备,以便灵活应用.

练习册系列答案
相关题目
(2011?包河区一模)某校化学兴趣小组为了解碳酸氢钠粉末(NaHCO3)的化学性质,进行了如图实验探究,请你一起参与他们的活动.该小组成员将少量碳酸氢钠粉末置于下图装置的试管中,充分加热至反应完全,发现试管口出现无色液体,澄清石灰水变浑浊,且试管底部有白色固体残余.根据质量守恒定律,两位同学提出以下猜想:
(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:
根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:
①澄清石灰水变浑浊的反应方程式:;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
根据甲同学的猜想与验证,乙同学认为甲的结论不准确,因为;
③以下是乙同学设计的实验:
④根据以上实验探究内容,写出碳酸氢钠受热分解的化学方程式:.
(4)讨论交流:
你还能设计不同的实验方案来验证乙同学的猜想吗?如果能你将获得激励分4分

(1)提出问题:残余白色固体的成分是什么?
(2)猜想与假设:
根据化学反应前后元素种类不变,两位同学提出以下猜想:
【猜想一】甲同学:“白色固体是氢氧化钠(NaOH)”;
【猜想二】乙同学:“白色固体是碳酸钠(Na2CO3)”.
(3)实验与结论:
①澄清石灰水变浑浊的反应方程式:;
②为了验证自己的猜想,甲同学设计了以下方案并实验验证:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量残余固体于试管中,加入适量的水使之溶解,往试管中滴加2滴无色酚酞溶液,观察现象 | 溶液变红 | 白色固体是氢氧化钠 |
③以下是乙同学设计的实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量残余固体于试管中,加入适量,观察现象 | 试管中产生大量气泡 |
(4)讨论交流:
你还能设计不同的实验方案来验证乙同学的猜想吗?如果能你将获得激励分4分
| 实验步骤 | 实验现象 | 实验结论 |