��Ŀ����
2��2012��9��7�գ�������ͨ�����ط����ϴ������1����������ʱ���������ǵ�һλ�ġ���Ϊ�Ѿ����ڷ����µ��Ҵ��ߣ���Ԯ�ӵ����������Ѿ�Ȯ���Ѿ�Ȯ�ܸ������巢������ζ�����Ҵ��ߣ����۵ĽǶȷ����Ѿ�Ȯ�ܷ����Ҵ��ߵ�ԭ����B��
A�����ӵ�������С B�������ڲ����˶� C�����Ӽ��м��
��2������������ԭ�е�ˮԴ���ƻ�����ˮԴ����ʹ�������ܳ�Ϊ����ˮ��
�پ���ˮʱ������ͨ���������������ۡ�������Ȼ��ͨ�����ˣ���������ƣ���ʵ�֣�
��Ҫɱ��ϸ������ͨ�������������ɱ��ϸ�������ܵõ�����������ˮ��
��3���ճ��������������Ӳˮ����ˮ�������ʵ�鲽��������ȡ��Ʒ�������Թܻ��ձ��У������Թܻ��ձ��м������ˮ���������ĭ�ࡢ��������Ϊ��ˮ����ĭ�١������࣬��Ϊ��Ӳˮ��
��4����Щ��ѧ��Ԥ�ԣ������������һ��ˮ������������ᡱ����仰��ʾ����Ӧ��������ˮ��Դ����ʶ��һ�ǽ�Լ��ˮ�����Ƿ�ֹˮ����Ⱦ�������һ����Լ��ˮ��������ϴ�˵�ˮ���������ȣ������𰸾��ɣ���
���� ��1�����ݷ��ӵĻ����������������ڲ����˶����Լ������ʵ���з����жϼ��ɣ�
��2�����ݹ��˿��Գ�ȥ�����Թ���������н��
��3�����������п��÷���ˮ����Ӳˮ����ˮ���н��
��4�����ݽ�Լ��ˮ�ķ������н��
��� �⣺��1���Ѿ�Ȯ�������巢������ζ�����Ҵ��ߣ�˵��������ζ�ķ����ڲ��ϵ��˶�����������ɢ�����Ѿ�Ȯ�ᵽ��
��2�����˿��Գ�ȥ�����Թ�����������Ի�ˮʱ������ͨ���������������ۡ�������Ȼ��ͨ�����˶�ʵ�֣�Ҫɱ��ϸ������ͨ����в�������ɱ��ϸ�������ܵõ�����������ˮ��
��3�������п��÷���ˮ����Ӳˮ����ˮ����������Ӳˮ����ˮ��ʵ�鲽��������ȡ��Ʒ�������Թܻ��ձ��У������Թܻ��ձ��м������ˮ���������ĭ�ࡢ��������Ϊ��ˮ����ĭ�١������࣬��Ϊ��Ӳˮ��
��4����Щ��ѧ��Ԥ�ԣ������������һ��ˮ������������ᡱ����仰��ʾ����Ӧ��������ˮ��Դ����ʶ��һ�ǽ�Լ��ˮ�����Ƿ�ֹˮ����Ⱦ����Լ��ˮ��������ϴ�˵�ˮ���������ȣ�
�ʴ�Ϊ����1��B����2���ٹ��ˣ� ����У� ��3��ȡ��Ʒ�������Թܻ��ձ��У������Թܻ��ձ��м������ˮ���������ĭ�ࡢ��������Ϊ��ˮ����ĭ�١������࣬��Ϊ��Ӳˮ����4��ϴ�˵�ˮ���������ȣ�
���� ������Ҫ���������ʵ����ʺ;���ˮ��������ݣ������������е�֪ʶ���У�

 ij���������ð�������Ĵ����Ʒ�к��������Ȼ������ʣ����Ʒ��װ����ע����
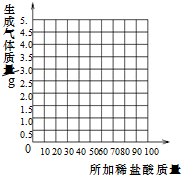
ij���������ð�������Ĵ����Ʒ�к��������Ȼ������ʣ����Ʒ��װ����ע����̼���ơ�96%��Ϊ�ⶨ�ò�Ʒ�к�̼���Ƶ���������������������ʵ�飺ȡ11.0g������Ʒ�����ձ��У��Ƶ��ձ�����ʢ������Ʒ��������Ϊ158.0g���ٰ�100gϡ����ƽ���ֳ��ķ����μ��뵽���ձ��У�ÿ�ξ���ַ�Ӧ��ʵ�����ݼ�¼���£�
| ��������Ĵ��� | ��һ�� | �ڶ��� | ������ | ���Ĵ� |
| �ձ�����ʢ����������/g | 181.2 | 204.4 | 228.6 | 253.6 |
��1����һ�μ���ϡ�����ַ�Ӧ�����ɶ�����̼��������1.8�ˣ�
��2���ò�Ʒ��̼���Ƶ����������Ƿ�ϸ�
��Ҫ��д��������̣������ȷ��0.1%��
��3������������������������������ȷ��0.1%��
��4������ʵ�����ݣ����ұߵ�����ֽ�ϻ��Ƴ�����ϡ������������������������ϵ�����ߣ���д����Ҫ�ļ�����̣�
| A�� | ����������ͭ��Ӧ��IJ�����������ϴ��Cu+2HNO3�TCu��NO3 ��2+H2�� | |
| B�� | ����ϡ���ᷴӦ��ȡ������2Fe+6HCl�T2FeCl3+3 H2�� | |
| C�� | ʯ�ҽ�Ĩǽ���ñ�Ӳ��Ca��OH��2+CO2�TCaCO 3��+H2O | |
| D�� | ʵ�����Ʊ�������2H2O=2H2��+O2�� |
| A�� | ����к� | B�� | ����ʯ��ʯ | ||
| C�� | ����������ͭ��Һ�� | D�� | ��ʯ����ˮ��Ӧ |

 ��̼ԭ�ӵĺ˵����Ϊ6��
��̼ԭ�ӵĺ˵����Ϊ6��
 ��ͼ�ǻ���̿��ˮ��ʾ��ͼ���ش�
��ͼ�ǻ���̿��ˮ��ʾ��ͼ���ش�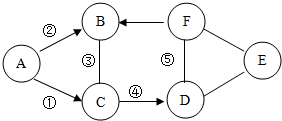 A��B��C��D��E��F���dz��л�ѧ���������ʣ�A��C����άϵ������������Ҫ�����ʣ�B�����ڹ�����ú��������壬D�����ڱ�����ľ����ֹ���ˣ�����ֹ�������ѣ�E������θҺ�к��е��ᣬ����֮���ת����ϵ��ͼ��ʾ������-����ʾ���˵������ܷ�����ѧ��Ӧ����������ʾ����֮���ת����ϵ����
A��B��C��D��E��F���dz��л�ѧ���������ʣ�A��C����άϵ������������Ҫ�����ʣ�B�����ڹ�����ú��������壬D�����ڱ�����ľ����ֹ���ˣ�����ֹ�������ѣ�E������θҺ�к��е��ᣬ����֮���ת����ϵ��ͼ��ʾ������-����ʾ���˵������ܷ�����ѧ��Ӧ����������ʾ����֮���ת����ϵ����