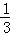题目内容
氨碱法制纯碱的工业流程如下:

(1)最终所得纯碱主要成分的化学式是 ,它属于 (酸、碱或盐),该产品易溶于水,溶液显 性;
(2)由步骤③所得的碳酸氢钠在生产和生活中有许多重要用途,在医疗上,它是治疗 过多的药剂之一;
(3)试写出步骤④中发生反应的化学方程式 .
| 纯碱的制取;常用盐的用途;盐的化学性质;常见的氧化物、酸、碱和盐的判别;书写化学方程式、文字表达式、电离方程式. | |
| 专题: | 常见的盐 化学肥料. |
| 分析: | (1)向饱和食盐水中加入氨气、二氧化碳后,能够生成碳酸氢钠和氯化铵,相同条件下碳酸氢钠的溶解度小于氯化铵的溶解度,因此碳酸氢钠会析出,加热碳酸氢钠能够生成碳酸钠、水和二氧化碳,从而得到纯碱; (2)碳酸氢钠能和稀盐酸反应生成氯化钠、水和二氧化碳; (3)根据反应物、生成物、反应条件及其质量守恒定律可以书写反应的化学方程式. |
| 解答: | 解:(1)最终所得纯碱的主要成分是碳酸钠,碳酸钠的化学式是Na2CO3,碳酸钠是由钠离子和碳酸根离子组成的化合物,属于盐,碳酸钠溶于水时溶液显碱性. 故填:Na2CO3;盐;碱. (2)碳酸氢钠无毒,能够和胃液中的稀盐酸反应,因此可以用于治疗胃酸过多. 故填:胃酸. (3)碳酸氢钠受热分解的化学方程式为:2NaHCO3Na2CO3+H2O+CO2↑. 故填:2NaHCO3Na2CO3+H2O+CO2↑. |
| 点评: | 化学来源于生产、生活,也服务于生产、生活,要学好化学知识,为生产、生活服务. |

 七彩题卡口算应用一点通系列答案
七彩题卡口算应用一点通系列答案下列除去物质所含杂质的方法不正确的是(括号内为杂质)( )
|
| A. | MnO2(KCl),加足量水溶解,过滤,洗涤,干燥 |
|
| B. | N2(O2),将气体缓缓通过灼热的铜网 |
|
| C. | FeSO4溶液(CuSO4),加过量Fe粉,过滤 |
|
| D. | CO2(HCl),通过NaOH溶液后用浓硫酸干燥 |
下列说法中正确的是( )
|
| A. | 尝药品的味道 |
|
| B. | 实验剩余的药品放回原试剂瓶中 |
|
| C. | 加热试管里的液体时,试管口不能朝着自己或他人 |
|
| D. | 稀释浓硫酸时,把水注入浓硫酸,并不断搅拌 |
下列有关仪器使用或用途的叙述中正确的是( )
|
| A. | 托盘天平,称量时把称量物放在右盘,砝码放在左盘 |
|
| B. | 胶头滴管,向试管中滴加液体时应将胶头滴管伸入试管内 |
|
| C. | 酒精灯,熄灭酒精灯时可用嘴吹灭 |
|
| D. | 试管:加热时所盛液体体积 |
在研究酸和碱的化学性质时,某小组想证明稀硫酸与氢氧化钠溶液混合后,虽然无明显现象,但确实发生了化学反应,试与他们一起完成实验方案的设计,实施和评价,并得出有关结论.
(1)探究稀硫酸与氢氧化钠溶液的反应:
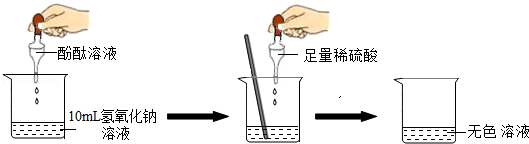
当滴入几滴酚酞试液后,溶液由无色变为 色,根据上述实验中颜色变化,可确定稀硫酸与氢氧化钠溶液发生了化学变化,反应的化学方程式为:.
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:
根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量,同学们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,请你判断并分析:
| 实验方案 | 实验步骤 | 实验现象 | 实验结论 |
| 方案一 | 取样,滴入适量的氯化钡溶液 | 出现白色沉淀 | 稀硫酸过量 |
| 方案二 | 取样,滴入几滴紫色石蕊试液 | 溶液变红 | 稀硫酸过量 |
上述设计的实验方案中,正确的是 (填“方案一”或“方案二”)
另外一个实验方案错误的原因是 ;
请你设计一个确定稀硫酸是否过量的实验方案,你选用的药品是 ,实验现象及结论是 .
 不得超过试管容积的
不得超过试管容积的