题目内容
某实验小组的同学用氢氧化钙溶液和盐酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会儿后,发现忘记了滴加指示剂.此时,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质的成分进行探究.
【提出问题】该烧杯内反应后溶液中的溶质是什么?
【进行猜想】猜想一:溶质可能是CaCl2与Ca(OH)2;猜想二:溶质可能只是CaCl2;猜想三:
【查阅资料】氯化钙溶液 CaCl2 呈中性
【实验与结论】
实验1:取了少量烧杯内反应后的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡.
实验现象: ,结论:猜想一不正确.
实验2:取了少量烧杯内反应后的溶液于另外一支试管中,加入一小段镁条.
实验现象: ,结论:猜想二不正确,猜想三正确.
【反思与扩展】
在分析化学反应后所得物质成分时,除了考虑生成物外还需要考虑 .
【提出问题】该烧杯内反应后溶液中的溶质是什么?
【进行猜想】猜想一:溶质可能是CaCl2与Ca(OH)2;猜想二:溶质可能只是CaCl2;猜想三:
【查阅资料】氯化钙溶液 CaCl2 呈中性
【实验与结论】
实验1:取了少量烧杯内反应后的溶液于试管中,并向试管中滴加几滴无色酚酞试液,振荡.
实验现象:
实验2:取了少量烧杯内反应后的溶液于另外一支试管中,加入一小段镁条.
实验现象:
【反思与扩展】
在分析化学反应后所得物质成分时,除了考虑生成物外还需要考虑
考点:实验探究物质的组成成分以及含量,酸的化学性质,碱的化学性质,盐的化学性质
专题:科学探究
分析:【进行猜想】猜想③根据反应的程度进行猜想:恰好反应、一种物质完全反应,另一种物质有剩余;
【实验与结论】(1)根据酚酞遇碱变红来进行分析;
(2)根据盐酸的化学性质进行分析;
【反思与扩展】根据实验的结论进行反思.
【实验与结论】(1)根据酚酞遇碱变红来进行分析;
(2)根据盐酸的化学性质进行分析;
【反思与扩展】根据实验的结论进行反思.
解答:解:【进行猜想】猜想:反应可能是恰好反应,只有氯化钙、也可能是一种物质完全反应,另一种物质有剩余,若氢氧化钙过量,则含有氢氧化钙和氯化钙;若盐酸过量,则含有盐酸和氯化钙;
【实验与结论】(1)因为酚酞遇碱会变红色,无色酚酞溶液不变色,说明反应后的溶液不呈碱性,而猜想①中含有Ca(OH)2,溶液应呈碱性,所以猜想一不正确;
(2)镁和盐酸反应会生成氯化镁和氢气,所以实验现象是:有气泡产生,所以猜想二不正确,猜想三正确;
【反思与扩展】因为反应可能是完全反应,也可能是其中的一种反应物过量,因此在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
故答案为:【进行猜想】CaCl2、HCl;
【实验与结论】无色酚酞溶液不变色,有气泡产生;
【反思与扩展】反应物用量.
【实验与结论】(1)因为酚酞遇碱会变红色,无色酚酞溶液不变色,说明反应后的溶液不呈碱性,而猜想①中含有Ca(OH)2,溶液应呈碱性,所以猜想一不正确;
(2)镁和盐酸反应会生成氯化镁和氢气,所以实验现象是:有气泡产生,所以猜想二不正确,猜想三正确;
【反思与扩展】因为反应可能是完全反应,也可能是其中的一种反应物过量,因此在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量.
故答案为:【进行猜想】CaCl2、HCl;
【实验与结论】无色酚酞溶液不变色,有气泡产生;
【反思与扩展】反应物用量.
点评:本题考查了酸碱中和反应以及实验设计的能力,设计实验时,可以从反应后的产物和其有关的性质着手.

练习册系列答案
 新编小学单元自测题系列答案
新编小学单元自测题系列答案 字词句段篇系列答案
字词句段篇系列答案
相关题目
如图是某化学反应的微观示意图,相关分析正确的是( )


| A、两种单质反应生成一种化合物和另一种单质 |
| B、参加反应的两种物质的物质的量之比为1:1 |
| C、该化学反应属于分解反应 |
| D、该化学反应的生成物可能是氧化物 |
T℃时将少量生石灰加到一定质量的饱和澄清石灰水中,溶液的温度升高,再将其恢复到T℃(不考虑水的蒸发),下列四位同学对变化后溶液的分析错误的是( )
| A、溶质的质量分数与原溶液的相同 |
| B、溶剂的质量比原溶液的减少了 |
| C、溶质的质量与原溶液的相同 |
| D、析出固体后的溶液是不饱和溶液 |
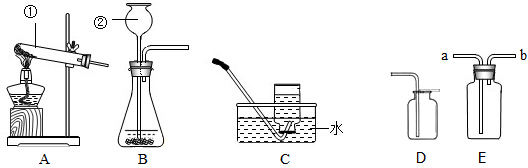

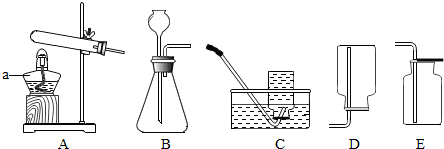
 O2和CO2是自然界中生命活动不可缺少的两种气体,两位同学有如下讨论:
O2和CO2是自然界中生命活动不可缺少的两种气体,两位同学有如下讨论:
 某校化学实验兴趣小组想了解水的组成,他们做了如下实验:
某校化学实验兴趣小组想了解水的组成,他们做了如下实验: