题目内容
甲、乙两种固体物质的溶解度曲线如图所示,请回答问题:
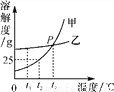
(1)t1 ℃时,甲、乙两种物质的溶解度大小关系为甲________(填“<”“>”或“=”)乙;
(2)P点的含义___________;
(3)t2 ℃时,把20 g固体甲放入50 g水中,充分搅拌,所得溶液的质量是________g;
(4)欲将t2 ℃时乙物质的不饱和溶液变为该温度下的饱和溶液,可采取的一种方法是________________;
(5)如果甲物质中含有少量乙物质,若要提纯甲,一般采用________的方法。
< t3 ℃时,甲、乙两物质的溶解度相等 62.5 增加溶质或恒温蒸发溶剂 降温结晶 【解析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。 (1)据图可以看出,t1℃时,甲、乙两...
练习册系列答案
相关题目
某化学兴趣小组为了测定镁铜合金中镁的质量分数,取了该合金样品2.0g并将30稀硫酸分6次加入样品中。充分反应后过滤,称重,得到相关数据如下:
稀硫酸的用量 | 剩余固体质量 | 稀硫酸的用量 | 剩余固体质量 |
第一次 5 g | m | 第四次 5 g | 0.8 g |
第二次 5 g | 1.4g | 第五次 5 g | 0.6g |
第三次 5 g | 1.1g | 第六次 5 g | 0.6g |
(1) 表格中m的数值为 ________。
(2) 样品中镁的质量分数为 ________ 。
(3) 求所用硫酸溶液中溶质质量分数为_____________。
1.7g 70% 24.5% 【解析】(1)由表可知,每5g的稀硫酸可以反应0.3g的固体,故m=1.4g+0.3g=1.7g (2)由表可知2.0g样品中铜的质量为0.6g,故镁的质量为1.4g,故样品中镁的质量分数为=70% (3)设反应硫酸质量为x 第三次反应的镁的质量为1.4克-1.1克=0.3克 Mg+ H2SO4 = MgSO4 + H2↑ 24 9...


