题目内容
2.根据下列装置回答.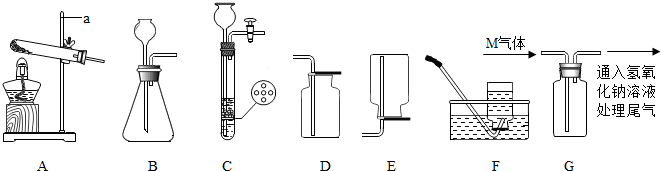
①仪器a的名称是铁架台;
②实验室用氯酸钾和二氧化锰的混合物制取氧气,可选择的一组装置是AD或AF(填编号),写出反应的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
③用大理石和稀盐酸制取二氧化碳,反应的化学方程式是CaCO3+2HCl=CaCl2+CO2↑+H2O.符合启普发生器原理的装置是C(填编号);
④图G是收集M气体的实验装置,据此可推测出M具有的性质为AC(填字母序号).
A.M气体的密度大于空气的密度 B.M气体的密度小于空气的密度
C.M气体溶于水所得溶液呈酸性 D.M气体溶于水所得溶液呈碱性.
分析 据常用仪器的名称,制取装置包括加热和不需加热两种,如果用双氧水制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取,二氧化碳密度比空气的密度大,能溶于水,因此只能用向上排空气法收集.G装置收集气体,长进短出,则该气体密度比空气大,尾气用氢氧化钠溶液处理,则该气体显酸性.
解答 解:①仪器a的名称是铁架台;
②氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集,反应的方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
③二氧化碳的实验室制法是用稀盐酸与大理石(或石灰石.其主要成分都是碳酸钙)反应来制取.其反应原理是CaCO3+2HCl=CaCl2+CO2↑+H2O.;C装置可控制反应的发生和停止,故符合启普发生器原
理;
④G装置收集气体,长进短出,则该气体密度比空气大,尾气用氢氧化钠溶液处理,则该气体显酸性.
故答案为:①铁架台;(2)AD或AF、2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
③CaCO3+2HCl=CaCl2+CO2↑+H2O、C;④AC.
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中

 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案| A. |  加热一定量高锰酸钾固体制取氧气 | |
| B. |  用一定量的双氧水制取氧气 | |
| C. |  一定质量的锌粒与足量稀盐酸反应 | |
| D. |  在恒温条件下往硝酸钾饱和溶液中继续加入硝酸钾固体 |
| A. | +2 | B. | -2 | C. | +4 | D. | +3 |
| A. | 2个氢分子2H | B. | 4个水分子 4H2O | C. | 钴元素CO | D. | 3个氧原子O3 |
| A | B |
| ①FeO、CuO、C、Fe只用一种试剂无法鉴别--正确 ②NaOH、NaCl、FeCl3不增加其他试剂也能鉴别出来--正确 ③用氯化钡溶液可以区分稀硫酸和稀盐酸--正确 | ①NaNO3、HCl、Na2SO4能在PH=1的溶液中大量共存--正确 ②Fe3+、Cl-、SO42-能共存于同一无色溶液中--错误 ③(NH4)2 SO4、NaOH、Na2SO4能同一溶液中共存--正确 |
| C | D |
| ①CaCl2中混有CaCO3,可以通过加水、过滤、蒸发操作除去--正确 ②CO中混有CO2和水蒸汽,可以将混合气体先通过浓硫酸,再通过氢氧化钠溶液除去--错误 ③NaOH 溶液中Na2CO3,可以加入适量Ca (OH)2溶液,再过滤除去--正确 | ①在某溶液中,加入氯化钡溶液和稀硝酸产生白色沉淀,该溶液中一定含有硫酸根离子--正确 ②测得某溶液的PH=9,则该溶液一定为碱的溶液--正确 ③在稀盐酸和氢氧化钠溶液的混合物中滴加无色酚酞溶液不变色,说明两者恰好反应完.--正确 |
| A. | A | B. | B | C. | C | D. | D |